Hvordan påvirker aktiveringsenergi kemiske reaktioner?
1. Reaktionshastighed:
* Højere aktiveringsenergi =langsommere reaktion: En højere aktiveringsenergi betyder, at der kræves mere energi for at reaktanter skal nå overgangstilstand og danne produkter. Dette resulterer i en langsommere reaktionshastighed.
* lavere aktiveringsenergi =hurtigere reaktion: En lavere aktiveringsenergi kræver mindre energi til, at reaktionen fortsætter, hvilket fører til en hurtigere reaktionshastighed.
2. Reaktionshastighedskonstant:
* Aktiveringsenergi er direkte relateret til hastighedskonstanten (k) for en reaktion gennem Arrhenius-ligningen: k =a * exp (-ea/rt) , hvor:
* k er hastighedskonstanten
* A er den præ-eksponentielle faktor
* Ea er aktiveringsenergien
* R er den ideelle gaskonstant
* T er temperaturen
3. Ligevægtskonstant:
* Mens aktiveringsenergi direkte påvirker reaktionshastigheden, påvirker den ikke ligevægtskonstanten (K). Ligevægtskonstanten afhænger af forskellen i energi mellem reaktanter og produkter, ikke af aktiveringsenergien.
4. Katalysatorer:
* Katalysatorer fungerer ved at sænke aktiveringsenergien i en reaktion. De giver en alternativ reaktionsvej med en lavere energibarriere og øger derved reaktionshastigheden uden at påvirke ligevægten.
5. Temperaturafhængighed:
* Forøgelse af temperaturen giver mere energi til reaktantmolekyler, hvilket gør det lettere for dem at overvinde aktiveringsenergibarrieren. Dette fører til en eksponentiel stigning i reaktionshastigheden.
Kortfattet:
Aktiveringsenergi er en afgørende faktor, der bestemmer hastigheden af en kemisk reaktion. En højere aktiveringsenergi fører til en langsommere reaktion, mens en lavere aktiveringsenergi resulterer i en hurtigere reaktion. Katalysatorer kan fremskynde reaktionerne ved at sænke aktiveringsenergien, mens temperaturændringer påvirker reaktionshastigheden ved at ændre den tilgængelige energi for at overvinde aktiveringsenergibarrieren.
Sidste artikelHvad er råmaterialerne i fotosyntesen?
Næste artikelOxygenatomer i iltgassen produceret af fotosyntesen kommer fra hvad?
 Varme artikler
Varme artikler
-
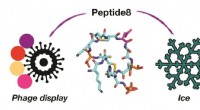 Brug af fager til at opdage nye frostvæskeproteinerBrug af vira (fagdisplay) til at identificere det ene molekyle i en milliard (peptid8), der styrer dannelsen af is. Kredit:University of Warwick Kontrollere, og afbødning af virkningerne af isvæ
Brug af fager til at opdage nye frostvæskeproteinerBrug af vira (fagdisplay) til at identificere det ene molekyle i en milliard (peptid8), der styrer dannelsen af is. Kredit:University of Warwick Kontrollere, og afbødning af virkningerne af isvæ -
 Omdannelse af atmosfærisk kulstof til industrielt anvendelige materialerKredit: RSC Advances (2021). DOI:10.1039/d1ra00954k Planter er uden sidestykke i deres evne til at fange CO 2 fra luften, men denne fordel er midlertidig, som restafgrøder frigiver kulstof tilb
Omdannelse af atmosfærisk kulstof til industrielt anvendelige materialerKredit: RSC Advances (2021). DOI:10.1039/d1ra00954k Planter er uden sidestykke i deres evne til at fange CO 2 fra luften, men denne fordel er midlertidig, som restafgrøder frigiver kulstof tilb -
 Integreret lab-on-a-chip bruger smartphone til hurtigt at opdage flere patogenerSystemet bruger en kommerciel smartphone til at erhverve og fortolke realtidsbilleder af en enzymatisk amplifikationsreaktion, der finder sted i en siliciummikrofluidisk chip, der genererer grøn fluor
Integreret lab-on-a-chip bruger smartphone til hurtigt at opdage flere patogenerSystemet bruger en kommerciel smartphone til at erhverve og fortolke realtidsbilleder af en enzymatisk amplifikationsreaktion, der finder sted i en siliciummikrofluidisk chip, der genererer grøn fluor -
 Forskere udvikler værktøj til hurtig diagnosticering af bakterielle infektionerMohammad Zarifi, en assisterende professor ved UBC Okanagan, viser sin lille biosensor, der kan bruges til at stille en realtidsdiagnose af en bakteriel infektion. Kredit:UBC Okanagan Ved hjælp af
Forskere udvikler værktøj til hurtig diagnosticering af bakterielle infektionerMohammad Zarifi, en assisterende professor ved UBC Okanagan, viser sin lille biosensor, der kan bruges til at stille en realtidsdiagnose af en bakteriel infektion. Kredit:UBC Okanagan Ved hjælp af
- Hvilken effekt har geografi på klimaet?
- Einstein vs kvantemekanik, og hvorfor han ville være en konvertit i dag
- Forskere visualiserer direkte produkter af gensidig neutralisering af hydronium og hydroxid
- Nye angreb på grafikprocessorer bringer brugernes privatliv i fare
- USA afbryder russisk botnet på 500, 000 hackede routere
- Strengene blev eksperimentelt observeret for første gang


