Hvad vil sandsynligvis ske med et enzym, hvis det er placeret i miljøet, der er for surt eller grundlæggende?
* enzymer er meget specifikke: De har en meget specifik tredimensionel form (konformation), der giver dem mulighed for at binde til deres underlag og katalysere en specifik reaktion. Denne form er afgørende for deres funktion.
* ph påvirker proteinstruktur: Proteiner, inklusive enzymer, består af aminosyrer. Disse aminosyrer har sidekæder, der kan oplades (positive eller negative) afhængigt af pH i miljøet.
* sure miljøer (lav pH): Overskydende H+ -ioner i sure miljøer forstyrrer de elektrostatiske interaktioner mellem aminosyresidekæder, hvilket fører til ændringer i proteinets form.
* Grundlæggende miljøer (høj pH): Overskydende OH-ioner forstyrrer også disse elektrostatiske interaktioner, hvilket forårsager ændringer i proteinets form.
* denaturering: Når enzymets form ændres markant på grund af ekstrem pH, mister det sin evne til at binde til underlaget og katalysere reaktionen. Dette funktionstab kaldes denaturering.
Tænk på det sådan: Forestil dig et enzym som en lås og dets underlag som en nøgle. Nøglen har en bestemt form, der passer perfekt ind i låsen. Hvis låsen er bøjet ud af form (denatureret) af en ekstrem pH, vil nøglen ikke længere passe, og låsen kan ikke åbne (enzymet kan ikke katalysere reaktionen).
Konsekvenser af denaturering:
* tab af funktion: Enzymet kan ikke længere udføre sin biologiske rolle.
* Potentiel skade: I nogle tilfælde kan denaturerede enzymer blive skadelige for cellen eller organismen.
Vigtig note: Hvert enzym har et optimalt pH -interval, hvor det fungerer bedst. Uden for dette interval bliver enzymet gradvist mindre aktivt, indtil det denaturerer.
 Varme artikler
Varme artikler
-
 Nyt upcycling-system til kommercielle polyestereForskere har udviklet en one-shot-proces til at omdanne almindeligt tilgængelige polymere plastik, såsom polyestere, til meget funktionelle materialer kaldet vitrimerer, der let kan genanvendes til ny
Nyt upcycling-system til kommercielle polyestereForskere har udviklet en one-shot-proces til at omdanne almindeligt tilgængelige polymere plastik, såsom polyestere, til meget funktionelle materialer kaldet vitrimerer, der let kan genanvendes til ny -
 Pulserne stiger, da ny undersøgelse afslører plantens hemmeligheder, der holder folk i roBeroligende indflydelse -- Indisk Snakeroot. Kredit:John Innes Center Kemiske hemmeligheder for en plante, der er blevet brugt gennem historien for dens beroligende virkning, er blevet afsløret i
Pulserne stiger, da ny undersøgelse afslører plantens hemmeligheder, der holder folk i roBeroligende indflydelse -- Indisk Snakeroot. Kredit:John Innes Center Kemiske hemmeligheder for en plante, der er blevet brugt gennem historien for dens beroligende virkning, er blevet afsløret i -
 Stigning af mandlige individer i stingless bier kolonier fører til dronninger dødUndersøgelse tyder på fremkomsten af hanbier med både faderligt og moderligt genetisk materiale ubalancer arbejdsstyrke i kolonier af Scaptotrigona depilis (fysogastrisk dronning inspicerer yngelc
Stigning af mandlige individer i stingless bier kolonier fører til dronninger dødUndersøgelse tyder på fremkomsten af hanbier med både faderligt og moderligt genetisk materiale ubalancer arbejdsstyrke i kolonier af Scaptotrigona depilis (fysogastrisk dronning inspicerer yngelc -
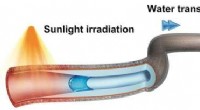 Hurtig kontrolleret transport af vanddråber via sollyspumpeKredit:Wiley Drevet af naturligt eller kunstigt sollys, en ny mikrorørspumpe transporterer vanddråber over lange afstande. Som rapporteret af kinesiske forskere i Journal Angewandte Chemie , pum
Hurtig kontrolleret transport af vanddråber via sollyspumpeKredit:Wiley Drevet af naturligt eller kunstigt sollys, en ny mikrorørspumpe transporterer vanddråber over lange afstande. Som rapporteret af kinesiske forskere i Journal Angewandte Chemie , pum
- Når mennesker ændrer miljøbalancen i økosystemer ændres aldrig?
- Nøgle fosforbaseret molekyle for liv på Jorden kan være kommet fra rummet
- Hvad er elektronkonfiguration af B3?
- Overproduktion truer Andes superfood fristed
- Strukturen, der omgiver æggeblommen og transporterer næringsstoffer til embryo, er hvad?
- Kejserpingviner marcherer mod udryddelse?


