Hvad er hydrofobt, og hvordan bestemmer du, om et molekyle hydrofobt?
hydrofobicitet forklaret:
Hydrofobe betyder "vandfryd". I kemi beskriver den tendensen for et molekyle til at afvise vand og undgå at danne bindinger med det. Dette sker på grund af molekylets ikke-polære karakter, hvilket betyder, at det har en afbalanceret fordeling af elektrisk ladning og har ikke en stærk positiv eller negativ ende som polære molekyler.
Tænk på det sådan: Forestil dig olie og vand. Olie er hydrofob. Det blandes ikke med vand, fordi det er ikke-polært, mens vand er polært. De afviser hinanden og danner separate lag.
hvordan man bestemmer, om et molekyle er hydrofobt:
Her er nogle nøglefaktorer, der skal overvejes:
1. Kemisk struktur:
* Ikke-polære bindinger: Molekyler med primært ikke-polære bindinger (som C-H-bindinger) har en tendens til at være hydrofobe.
* fravær af polære grupper: Se efter fraværet af grupper som -OH (hydroxyl), -NH2 (amin) eller -COOH (carboxyl), der fremstiller et molekyle polært.
* Tilstedeværelse af carbonhydridkæder: Lange kæder af kulbrinter (C-H) er karakteristiske for hydrofobe molekyler.
2. Molekylær form:
* sfærisk eller lineær form: Kompakte, sfæriske eller lineære former kan gøre det vanskeligt for vandmolekyler at interagere med molekylet.
* tilstedeværelse af voluminøse grupper: Store, voluminøse grupper kan hindre vandmolekyler i at nærme sig molekylet.
3. Opløselighed:
* uopløselighed i vand: Hydrofobe molekyler er generelt uopløselige i vand. De opløses muligvis i ikke-polære opløsningsmidler som olie eller ether.
Eksempler på hydrofobe molekyler:
* fedt og olier: Disse indeholder lange carbonhydridkæder.
* voks: Disse har lignende strukturer som fedt og olier.
* Ikke-polære gasser: Eksempler inkluderer metan, ethan og propan.
Forståelse af hydrofobicitet er vigtig på forskellige områder:
* biologi: Hydrofobe interaktioner er afgørende for proteinfoldning, cellemembranstruktur og lipidmetabolisme.
* Kemi: Hydrofobicitet spiller en rolle i vaskemidler, overfladeaktive stoffer og emulsionsdannelse.
* miljøvidenskab: Hydrofobe stoffer kan udgøre miljørisici på grund af deres vedholdenhed og potentiale for bioakkumulering.
Husk:
* Hydrofobicitet er ikke en absolut egenskab. Det er et relativt udtryk. Nogle molekyler kan være mere hydrofobe end andre.
* Nogle molekyler kan have både hydrofobe og hydrofile regioner, hvilket gør dem til amfipatiske.
Ved at overveje disse faktorer kan du få en bedre forståelse af molekylernes hydrofobe karakter og deres betydning i forskellige videnskabelige discipliner.
Sidste artikelHvad betyder ikke -polært molekyle?
Næste artikelHvordan sammenføjes aminosyrer?
 Varme artikler
Varme artikler
-
 En ny idé forbinder syntesen af ler og stofskiftets oprindelseIllustration, der forbinder syntesen af lerarter og metabolismens oprindelse. Kredit:Ruixin Zhou Spørgsmålet om, hvordan livet er begyndt, har fascineret forskere fra mange discipliner, og det v
En ny idé forbinder syntesen af ler og stofskiftets oprindelseIllustration, der forbinder syntesen af lerarter og metabolismens oprindelse. Kredit:Ruixin Zhou Spørgsmålet om, hvordan livet er begyndt, har fascineret forskere fra mange discipliner, og det v -
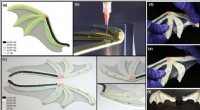 Forskere bryder ny vej inden for 3D-printet blød robotteknologi med det største udvalg af polymerh…(a) Illustration af det strukturelle design. (b) Direkte blæk-skrivning af hybridstrukturen. (c) Hærdet struktur (areal på ~90 cm 2 per vinge, membrantykkelse ~0,7 mm, total armtykkelse ~3,5 mm). (d
Forskere bryder ny vej inden for 3D-printet blød robotteknologi med det største udvalg af polymerh…(a) Illustration af det strukturelle design. (b) Direkte blæk-skrivning af hybridstrukturen. (c) Hærdet struktur (areal på ~90 cm 2 per vinge, membrantykkelse ~0,7 mm, total armtykkelse ~3,5 mm). (d -
 Forskere finder plads mellem polymerkæder påvirker energiomsætningKredit:Unsplash/CC0 Public Domain Et team ledet af FAMU-FSU College of Engineering-forskere har ny indsigt i molekyler, der ændrer deres form som reaktion på lys. Forskerne, der studerede azobens
Forskere finder plads mellem polymerkæder påvirker energiomsætningKredit:Unsplash/CC0 Public Domain Et team ledet af FAMU-FSU College of Engineering-forskere har ny indsigt i molekyler, der ændrer deres form som reaktion på lys. Forskerne, der studerede azobens -
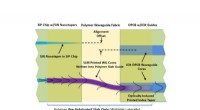 Nye polymermaterialer gør fremstilling af optiske sammenkoblinger nemmereForskere bruger, hvad de kalder en SmartPrint-proces til at udvikle nye polymermaterialer. Kredit:Robert Norwood, University of Arizona Forskere har udviklet nye polymermaterialer, der er ideelle t
Nye polymermaterialer gør fremstilling af optiske sammenkoblinger nemmereForskere bruger, hvad de kalder en SmartPrint-proces til at udvikle nye polymermaterialer. Kredit:Robert Norwood, University of Arizona Forskere har udviklet nye polymermaterialer, der er ideelle t


