Hvad er klamringen af et stof til et andet, dette gør vand til et især godt opløsningsmiddel?
Adhæsion sammen med samhørighed (Tiltrækningen mellem molekyler af det samme stof) gør vand til et særligt godt opløsningsmiddel. Her er hvorfor:
* Adhæsion til opløste stoffer: Vandmolekyler er meget polære, hvilket betyder, at de har en positiv og negativ ende. Dette giver dem mulighed for at danne stærke attraktioner (brintbindinger) med de polære ender af andre molekyler, som sukker eller salt. Denne attraktion hjælper med at trække de opløste molekyler fra hinanden og opløse dem.
* samhørighed til sig selv: Vandmolekyler har også stærke sammenhængende kræfter og danner brintbindinger med hinanden. Dette hjælper med at holde vandmolekylerne samlet sammen, selv når de prøver at omringe og opløse et opløst stof.
Sammenfattende giver kombinationen af stærk vedhæftning og samhørighed i vand det mulighed for effektivt at opløse en lang række stoffer, hvilket gør det til et fremragende opløsningsmiddel.
Sidste artikelHvilket molekyle holder på ilt i blodlegemer?
Næste artikelHvilket er en produktfotosyntese?
 Varme artikler
Varme artikler
-
 Ny teknik kan strømline lægemiddeldesignKredit:CC0 Public Domain Forskere har udviklet en proces, der kraftigt kan reducere arbejdet involveret i computerproteindesign, ifølge en undersøgelse i Proceedings of the National Academy of Sc
Ny teknik kan strømline lægemiddeldesignKredit:CC0 Public Domain Forskere har udviklet en proces, der kraftigt kan reducere arbejdet involveret i computerproteindesign, ifølge en undersøgelse i Proceedings of the National Academy of Sc -
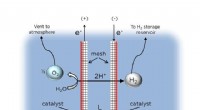 Ingeniører udvikler flydende solbrændstofrigg til havvandselektrolyseTo meshelektroder holdes i en smal adskillelsesafstand (L), og genererer H2- og O2 -gasser samtidigt. Den centrale innovation er den asymmetriske placering af katalysatoren på de udadvendte overflader
Ingeniører udvikler flydende solbrændstofrigg til havvandselektrolyseTo meshelektroder holdes i en smal adskillelsesafstand (L), og genererer H2- og O2 -gasser samtidigt. Den centrale innovation er den asymmetriske placering af katalysatoren på de udadvendte overflader -
 Forstå hvordan monomersekvens påvirker konduktans i molekylære ledningerForskere i Schroeder- og Moore-grupperne ved University of Illinois er interesserede i at bygge og studere kædemolekyler med høje præcisionsniveauer. På billedet fra venstre, Hao Yu, kandidatstuderend
Forstå hvordan monomersekvens påvirker konduktans i molekylære ledningerForskere i Schroeder- og Moore-grupperne ved University of Illinois er interesserede i at bygge og studere kædemolekyler med høje præcisionsniveauer. På billedet fra venstre, Hao Yu, kandidatstuderend -
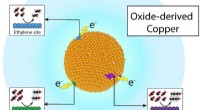 Kulbrændstoffer bliver grønne for vedvarende energiForskere ved Berkeley Lab og Joint Center for Artificial Photosynthesis har vist, at genanvendelse af kuldioxid til værdifulde kemikalier, såsom ethylen og propanol, og brændstoffer som ethanol, kan v
Kulbrændstoffer bliver grønne for vedvarende energiForskere ved Berkeley Lab og Joint Center for Artificial Photosynthesis har vist, at genanvendelse af kuldioxid til værdifulde kemikalier, såsom ethylen og propanol, og brændstoffer som ethanol, kan v
- Iværksættere sigter mod at stoppe spøgelsesfiskeri
- Hvad er organellen, der ændrer og pakker transporterer materialer ud af cellen?
- Hvad er energien fra en elektromagnetisk bølge med en frekvens 8x1012Hz?
- Hvordan kan du bestemme, om dine formørkelsesglas er sikre til at se solen under en formørkelse?
- Hvad gør en stjerne synlig?
- Hvad er menneskets rolle i at opretholde livet på jorden?


