Atomer, der er kendt som inerte eller ædle, gennemgår sjældent reaktioner, fordi?
Her er hvorfor:
* stabilitet: En fuld ydre skal af elektroner er den mest stabile elektronkonfiguration. Atomer stræber efter at opnå denne stabile tilstand, hvorfor de reagerer med andre atomer.
* Ingen grund til at dele: Noble gasser har allerede en komplet oktet (eller duet til helium) af elektroner, hvilket betyder, at de ikke behøver at vinde, miste eller dele elektroner med andre atomer for at blive stabile.
* Høj ioniseringsenergi: Noble gasser har høje ioniseringsenergier, hvilket gør det ekstremt vanskeligt at fjerne et elektron fra deres yderste skal. Dette bidrager yderligere til deres ureaktive karakter.
Eksempel: Helium har to elektroner, der fuldstændigt fylder sin første elektronskal. Dette gør det utroligt stabilt og resistent over for dannelse af kemiske bindinger.
Fortæl mig, hvis du gerne vil udforske dette yderligere!
 Varme artikler
Varme artikler
-
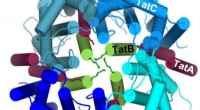 Biokemikere undersøger transporten af store proteiner gennem bakterielle cellemembranerFire TatC-molekyler (blå) danner en cirkel omkring fire TatB-molekyler (grøn) for at danne et hulrum i midten, hvori det protein, der skal transporteres, kan indsættes nedefra. Kredit: Journal of Biol
Biokemikere undersøger transporten af store proteiner gennem bakterielle cellemembranerFire TatC-molekyler (blå) danner en cirkel omkring fire TatB-molekyler (grøn) for at danne et hulrum i midten, hvori det protein, der skal transporteres, kan indsættes nedefra. Kredit: Journal of Biol -
 Eksoskeletal mikrostruktur af ekstremt hårde kokosnøddekrabbekløerSkematisk diagram, der viser tværsnitsstrukturerne af kokoskrabbekloens eksoskelet. Kredit:National Institute for Materials Science NIMS Research Center for Structural Materials og Okinawa Churash
Eksoskeletal mikrostruktur af ekstremt hårde kokosnøddekrabbekløerSkematisk diagram, der viser tværsnitsstrukturerne af kokoskrabbekloens eksoskelet. Kredit:National Institute for Materials Science NIMS Research Center for Structural Materials og Okinawa Churash -
 Bæredygtigt strukturelt materiale til plasterstatningDet cellulose nanofiber-afledte bulk CNFP-strukturmateriale og dets karakterisering. (a) Fotografi af CNFP i stor størrelse med et volumen på 320 × 220 × 27 mm3. (b) CNFPs robuste 3D nanofibernetværk.
Bæredygtigt strukturelt materiale til plasterstatningDet cellulose nanofiber-afledte bulk CNFP-strukturmateriale og dets karakterisering. (a) Fotografi af CNFP i stor størrelse med et volumen på 320 × 220 × 27 mm3. (b) CNFPs robuste 3D nanofibernetværk. -
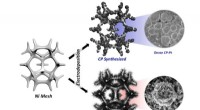 Ny teknik omdanner problemfrit ammoniak til grønt brintKredit:Ulsan National Institute of Science and Technology Et forskerhold ledet af professor Guntae Kim på School of Energy and Chemical Engineering ved UNIST har bebudet et gennembrud inden for te
Ny teknik omdanner problemfrit ammoniak til grønt brintKredit:Ulsan National Institute of Science and Technology Et forskerhold ledet af professor Guntae Kim på School of Energy and Chemical Engineering ved UNIST har bebudet et gennembrud inden for te


