Hvad er selvkondensation af aminosyrer?
* aminosyrer danner primært peptidbindinger: Den mest almindelige reaktion, der involverer aminosyrer, er dannelsen af peptidbindinger, hvor carboxylgruppen af en aminosyre reagerer med aminogruppen på en anden. Denne proces katalyseres af ribosomer og er grundlæggende for proteinsyntese.
* selvkondensering er energisk ugunstig: For at en enkelt aminosyre skal gennemgå selvkondensering, skulle carboxylgruppen reagere med sin egen aminogruppe. Denne reaktion er meget ugunstig, fordi:
* sterisk hindring: Amino- og carboxylgrupperne er tæt på hinanden, hvilket gør det vanskeligt for dem at reagere.
* ugunstig termodynamik: Reaktionen kræver fjernelse af et vandmolekyle, som er energisk ugunstig.
* Tilstedeværelse af andre aminosyrer: I biologiske systemer er aminosyrer sjældent til stede isoleret. De findes typisk i komplekse blandinger, hvilket gør selvkondensering endnu mindre sandsynlig.
Der er dog nogle undtagelser:
* Dipeptiddannelse: Under specifikke forhold kan nogle aminosyrer danne dipeptider gennem selvkondensering. Dette forekommer typisk i laboratorieindstillinger med høje koncentrationer af en enkelt aminosyre og ved hjælp af specifikke katalysatorer.
* cykliske peptider: Nogle cykliske peptider kan dannes gennem selvkondenseringsreaktioner, der involverer aminogruppen og sidekæden af den samme aminosyre. Disse reaktioner katalyseres ofte af enzymer.
Kortfattet: Mens aminosyrer kan gennemgå selvkondensering under specifikke forhold, er det ikke en almindelig eller signifikant proces i forbindelse med standardbiokemi. Dannelse af peptidbinding mellem forskellige aminosyrer er den primære mekanisme til proteinsyntese.
Sidste artikelHvad er et kemikalie i røde blodlegemer, der bærer ilt?
Næste artikelHvordan kommer iltmolekyler rundt om kroppen?
 Varme artikler
Varme artikler
-
 3-D gråskala digital lysudskrivning (g-DLP) materialer med høj funktionsgrad (FGM)Kompression af 3D anisotropt gitter. Kompression af det 3D isotrope gitter. Filmafspilningshastigheden er 10X fremspoling. Kompressionstestene blev udført i forskellige retninger. Kredit:Science Advan
3-D gråskala digital lysudskrivning (g-DLP) materialer med høj funktionsgrad (FGM)Kompression af 3D anisotropt gitter. Kompression af det 3D isotrope gitter. Filmafspilningshastigheden er 10X fremspoling. Kompressionstestene blev udført i forskellige retninger. Kredit:Science Advan -
 Designet protein switch tillader hidtil uset kontrol over levende cellerLOCKR er en molekylær kontakt lavet af flere interagerende dele:en nøgle (sort) låser op for et bur (grå), afsløre et bioaktivt peptid (gult), som kan interagere med andre molekyler i cellen. LÅS, e
Designet protein switch tillader hidtil uset kontrol over levende cellerLOCKR er en molekylær kontakt lavet af flere interagerende dele:en nøgle (sort) låser op for et bur (grå), afsløre et bioaktivt peptid (gult), som kan interagere med andre molekyler i cellen. LÅS, e -
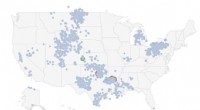 Magnetiske nanopartikler trækker værdifulde elementer fra vandkilderPotentielle lithiumkilder fra vand produceret i minedrift og petroleumsdrift, udtrykt som koncentration (parts per million). Data fra US Geological Survey, Produceret vanddatabase. Kredit:Pacific Nort
Magnetiske nanopartikler trækker værdifulde elementer fra vandkilderPotentielle lithiumkilder fra vand produceret i minedrift og petroleumsdrift, udtrykt som koncentration (parts per million). Data fra US Geological Survey, Produceret vanddatabase. Kredit:Pacific Nort -
 Kobberstearat lovende til tung olieoxidation, siger undersøgelseKredit:Kazan Federal University Kobbersalte har fundet plads i mange industrier fra lægemidler til landbrug, men de ses sjældent i petrokemi og olieudvinding. Nu, Forskere fra Kazan Federal Univer
Kobberstearat lovende til tung olieoxidation, siger undersøgelseKredit:Kazan Federal University Kobbersalte har fundet plads i mange industrier fra lægemidler til landbrug, men de ses sjældent i petrokemi og olieudvinding. Nu, Forskere fra Kazan Federal Univer
- Hvad er den potentielle energi på en 0,480 kg fugl, der sidder 22,8 m over jorden?
- Anti-hjælp retorik har indflydelse, men kun blandt fans af populistiske politikere
- Hvem udførte guldfolieeksperimentet for at opdage kerne?
- USA visner i en hedebølge på en eller anden måde fast omvendt
- Cellulose til fremstilling af avancerede materialer
- Hvordan nanopartikler flyder gennem miljøet


