Hvad er en atomobligation?
Typer af atomobligationer:
* ioniske bindinger: Disse bindinger dannes mellem atomer, der har en stor forskel i elektronegativitet (deres evne til at tiltrække elektroner). Det ene atom mister elektroner (bliver en positivt ladet ion), og den anden atom får elektroner (bliver en negativt ladet ion). De modsatte afgifter tiltrækker og danner en stærk elektrostatisk binding. Eksempler:NaCl (bordsalt), MgO (magnesiumoxid).
* kovalente obligationer: Disse bindinger dannes, når atomer deler elektroner for at opnå en stabil elektronkonfiguration. De delte elektroner tiltrækkes af kernerne i begge atomer og holder dem sammen. Kovalente bindinger kan være polære (ulige deling af elektroner, hvilket skaber en let positiv og negativ ende) eller ikke -polær (lige deling af elektroner). Eksempler:H2O (vand), CO2 (kuldioxid), methan (CH4).
* Metalliske obligationer: Disse bindinger forekommer mellem metalatomer. Valenselektronerne er delokaliseret, hvilket betyder, at de ikke er fastgjort til noget specifikt atom og kan bevæge sig frit gennem metalstrukturen. Dette "hav af elektroner" skaber stærke attraktioner mellem de positive metalioner, hvilket resulterer i et stærkt og formbart materiale. Eksempler:kobber (Cu), jern (Fe), guld (AU).
nøglefunktioner ved atombindinger:
* Energi: At danne obligationer frigiver energi, mens brud på obligationer kræver energi. Dette er grunden til, at kemiske reaktioner involverer energiændringer.
* styrke: Styrken af en binding afhænger af typen af binding og de involverede atomer. Ioniske bindinger er generelt stærkere end kovalente bindinger, som generelt er stærkere end metalliske bindinger.
* Retning: Nogle bindinger er retningsbestemte (kovalente bindinger), hvilket betyder, at de peger i specifikke retninger. Andre (metalliske obligationer) er ikke-retningsbestemte.
Hvorfor er atomobligationer vigtige?
Atombindinger er afgørende for forståelse:
* Egenskaber ved stof: Typen af binding bestemmer et stofs fysiske og kemiske egenskaber (f.eks. Smeltepunkt, ledningsevne, reaktivitet).
* Kemiske reaktioner: Kemiske reaktioner involverer brud og dannelse af bindinger, hvilket fører til oprettelse af nye stoffer.
* Strukturen af molekyler og materialer: Atombindinger dikterer, hvordan atomer arrangerer sig selv og danner molekyler og faste strukturer.
At forstå atombindinger er grundlæggende for kemi og hjælper os med at forklare opførelsen af alt fra enkle molekyler til komplekse materialer.
 Varme artikler
Varme artikler
-
 Solcellemateriale klarer sig bedre under trykAdskillelse af bromid og iodid i perovskitter resulterer i et inhomogent energilandskab, afbildet som bakker og dale. Ved højt tryk, jodidet og bromidet forbliver homogent fordelt, så perovskitterne b
Solcellemateriale klarer sig bedre under trykAdskillelse af bromid og iodid i perovskitter resulterer i et inhomogent energilandskab, afbildet som bakker og dale. Ved højt tryk, jodidet og bromidet forbliver homogent fordelt, så perovskitterne b -
 Vand, vand overalt - og det er mere mærkeligt, end du trorKredit:CC0 Public Domain Forskere ved University of Tokyo har brugt beregningsmetoder og analyse af nylige eksperimentelle data for at demonstrere, at vandmolekyler har to forskellige strukturer i
Vand, vand overalt - og det er mere mærkeligt, end du trorKredit:CC0 Public Domain Forskere ved University of Tokyo har brugt beregningsmetoder og analyse af nylige eksperimentelle data for at demonstrere, at vandmolekyler har to forskellige strukturer i -
 Røntgenstråler afslører en skjult egenskab, der fører til fejl i et lithium-ion batterimaterialeDe lithium-ion-batterier, der almindeligvis bruges til at drive elektriske busser og ledningsfrit værktøj og støvsugere, består ofte af milliarder af nanopartikler af lithiumjernfosfat, batterimateria
Røntgenstråler afslører en skjult egenskab, der fører til fejl i et lithium-ion batterimaterialeDe lithium-ion-batterier, der almindeligvis bruges til at drive elektriske busser og ledningsfrit værktøj og støvsugere, består ofte af milliarder af nanopartikler af lithiumjernfosfat, batterimateria -
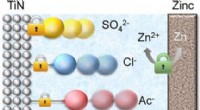 Zink-ion-hybridkondensatorer med ideelle anioner i elektrolytten viser ekstra lang ydelseKredit:Wiley Metal-ion hybrid kondensatorer kombinerer egenskaberne af kondensatorer og batterier. En elektrode bruger den kapacitive mekanisme, den anden redox-processer af batteritype. Forskere
Zink-ion-hybridkondensatorer med ideelle anioner i elektrolytten viser ekstra lang ydelseKredit:Wiley Metal-ion hybrid kondensatorer kombinerer egenskaberne af kondensatorer og batterier. En elektrode bruger den kapacitive mekanisme, den anden redox-processer af batteritype. Forskere
- Forskere opdager beviser for de seneste vandstrømme på Mars
- Hvor mange L er i 12,85 ml?
- Vanddyr, der hopper ud af vandet, inspirerer til springende robotter
- Forskere kortlægger global økonomi i samarbejde med LinkedIn
- Hvad er nogle andre videnskabelige ord, der betyder godt?
- Hvad betyder handlings- og reaktionskræfter i fysik?


