Hydrerede ioniske faste stoffer:definition, struktur og eksempler
Her er en oversigt:
* Ionisk forbindelse: En forbindelse dannet af den elektrostatiske tiltrækning mellem positivt ladede ioner (kationer) og negativt ladede ioner (anioner).
* Hydreret: Betyder, at vandmolekyler er inkorporeret i forbindelsens struktur.
* Krystalstruktur: Det organiserede, gentagne arrangement af ioner i et fast stof.
Sådan virker det:
1. Vandmolekyler interagerer med ionerne i den ioniske forbindelse gennem dipol-ion-interaktioner . Dette skyldes den polære natur af vandmolekyler, som har en positiv ende (brint) og en negativ ende (ilt).
2. Den positive ende af et vandmolekyle tiltrækker den negativt ladede anion, mens den negative ende af et vandmolekyle tiltrækker den positivt ladede kation.
3. Disse interaktioner er stærke nok til at holde vandmolekylerne på plads i krystalgitteret af ionforbindelsen.
Eksempler på hydrerede ioniske faste stoffer:
* Kobber(II)sulfatpentahydrat (CuSO₄·5H₂O) :Dette blå faststof har fem vandmolekyler forbundet med hver kobber(II)sulfatenhed.
* Natriumcarbonat decahydrat (Na₂CO₃·10H₂O) :Dette hvide faste stof indeholder ti vandmolekyler pr. formelenhed.
* Calciumchloriddihydrat (CaCl₂·2H2O) :Dette hvide faste stof har to vandmolekyler for hver calciumchloridenhed.
Karakteristika for hydrerede ioniske faste stoffer:
* De har ofte en anden farve sammenlignet med deres vandfri (vandfri) former. For eksempel er kobber(II)sulfatpentahydrat blåt, mens vandfrit kobber(II)sulfat er hvidt.
* De kan miste deres hydreringsvand ved opvarmning, hvilket resulterer i en ændring i farve og fysiske egenskaber. Denne proces kaldes dehydrering .
* De kan bruges til forskellige applikationer, såsom i lægemidler, landbrug og industrielle processer.
Opsummering, et hydreret ionisk fast stof er en ionisk forbindelse, hvor vandmolekyler er integreret i krystalstrukturen. Tilstedeværelsen af disse vandmolekyler påvirker forbindelsens egenskaber, herunder farve og stabilitet.
Sidste artikelKovalente bindinger i vand:stabilitet og dissociation
Næste artikelMineral Streak:Forståelse af farve og identifikation
 Varme artikler
Varme artikler
-
 Forskning guider fremtiden for kemisk genanvendelse af plastaffaldKredit:CC0 Public Domain Ny forskning fra Cornell College of Engineering har til formål at lette processen med kemisk genanvendelse - en ny industri, der kunne gøre affaldsprodukter tilbage til na
Forskning guider fremtiden for kemisk genanvendelse af plastaffaldKredit:CC0 Public Domain Ny forskning fra Cornell College of Engineering har til formål at lette processen med kemisk genanvendelse - en ny industri, der kunne gøre affaldsprodukter tilbage til na -
 Kemiske ingeniører fremmer produktionen af olefiner gennem beregningsmodelleringIllustration fra forsiden af ACS katalyse viser et vulkan aktivitetsplot, svarende til den, der er konstrueret i beregninger for at screene aktiviteten af forskellige steder på metaloxider, med to
Kemiske ingeniører fremmer produktionen af olefiner gennem beregningsmodelleringIllustration fra forsiden af ACS katalyse viser et vulkan aktivitetsplot, svarende til den, der er konstrueret i beregninger for at screene aktiviteten af forskellige steder på metaloxider, med to -
 Bedre adsorption af kemomedicin på målrettede leveringskapslerKredit:CC0 Public Domain Effekten af kemoterapibehandling afhænger af, hvor effektivt den når kræftceller. Øget målrettet levering kan betyde faldende bivirkninger. Forskere forbedrer metoder ti
Bedre adsorption af kemomedicin på målrettede leveringskapslerKredit:CC0 Public Domain Effekten af kemoterapibehandling afhænger af, hvor effektivt den når kræftceller. Øget målrettet levering kan betyde faldende bivirkninger. Forskere forbedrer metoder ti -
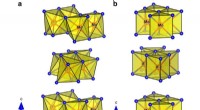 En ny metode til at udvinde brint fra vand mere effektivt for at opfange vedvarende energiKrystalstruktur og {MoTe}6 polyedre, der viser byggestenene i hver polymorf. en monoklinisk 1T′-MoTe2-fase og b hexagonal 2H-MoTe2-fase. Kredit: Naturkommunikation 10.1038/s41467-019-12831-0 En n
En ny metode til at udvinde brint fra vand mere effektivt for at opfange vedvarende energiKrystalstruktur og {MoTe}6 polyedre, der viser byggestenene i hver polymorf. en monoklinisk 1T′-MoTe2-fase og b hexagonal 2H-MoTe2-fase. Kredit: Naturkommunikation 10.1038/s41467-019-12831-0 En n
- Hvordan klimaændringer påvirker kulturarven
- Arbejder hen imod partnerbevidst humanoid robotstyring
- Kode i kinesisk overvågningsapp analyseret
- Holocaust-mindedag:COVID-19 ændrede, hvordan vi husker
- I hvilken højde vokser aspetræer?
- Nok ambition (og brint) kunne få Australien til 200% vedvarende energi


