Kovalente bindinger i vand:stabilitet og dissociation
Her er hvorfor:
* Kovalente bindinger er stærke: Kovalente bindinger involverer deling af elektroner mellem atomer. Disse delte elektroner skaber en stærk tiltrækning mellem atomerne og holder dem sammen.
* Vand er et polært opløsningsmiddel: Vandmolekyler har en delvis positiv ladning på brintatomerne og en delvis negativ ladning på iltatomet. Denne polaritet tillader vand at interagere med ioniske forbindelser og polære molekyler, men den har typisk ikke nok styrke til at bryde kovalente bindinger.
Der er dog undtagelser til denne regel:
* Svage kovalente bindinger: Nogle kovalente bindinger, især dem med lave elektronegativitetsforskelle mellem atomerne, kan brydes af vand. For eksempel kan bindingerne i nogle carboxylsyrer delvist dissociere i vand, hvilket fører til frigivelse af H+ ioner og dannelse af carboxylationer.
* Hydrolyse: Visse kovalente bindinger kan brydes af vand gennem en proces kaldet hydrolyse. Dette involverer tilføjelse af et vandmolekyle til bindingen, bryde det og danner to nye molekyler. For eksempel nedbryder hydrolysen af saccharose (bordsukker) det til glucose og fructose.
* Syre-base reaktioner: Stærke syrer som saltsyre (HCl) kan donere protoner (H+) til vand og bryde den kovalente binding i HCl-molekylet. Dette fører til dannelsen af hydroniumioner (H3O+) og chloridioner (Cl-), der effektivt dissocierer HCl-molekylet i vand.
Opsummering:
Kovalente bindinger er generelt meget stærke og dissocieres ikke let i vand. Der er dog undtagelser, der involverer svage kovalente bindinger, hydrolysereaktioner og stærke syre-basereaktioner.
 Varme artikler
Varme artikler
-
 Hvordan man nøjagtigt beregner opvarmningstid for ethvert materialeAf Lee Johnson — Opdateret 30. august 2022 Varmeoverførselsberegninger er en fast bestanddel i fysik og teknik. At vide, hvor lang tid det tager at hæve et objekts temperatur med en given mængde, kræ
Hvordan man nøjagtigt beregner opvarmningstid for ethvert materialeAf Lee Johnson — Opdateret 30. august 2022 Varmeoverførselsberegninger er en fast bestanddel i fysik og teknik. At vide, hvor lang tid det tager at hæve et objekts temperatur med en given mængde, kræ -
 Maskinlæringsmodel hjælper med at karakterisere forbindelser til lægemiddelopdagelseKredit:CC0 Public Domain Tandem massespektrometri er et kraftfuldt analytisk værktøj, der bruges til at karakterisere komplekse blandinger inden for lægemiddelopdagelse og andre områder. Nu, Purd
Maskinlæringsmodel hjælper med at karakterisere forbindelser til lægemiddelopdagelseKredit:CC0 Public Domain Tandem massespektrometri er et kraftfuldt analytisk værktøj, der bruges til at karakterisere komplekse blandinger inden for lægemiddelopdagelse og andre områder. Nu, Purd -
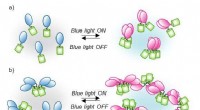 Proteinblanding under blåt lysSkema af CRY2PHR klyngemekanismen udløst af blåt lys. I dette optogenetiske system, CRY2-klynger (blå og pink) styres reversibelt af blåt lys. Hvis CRY2 er forbundet med fluorescerende proteiner (grøn
Proteinblanding under blåt lysSkema af CRY2PHR klyngemekanismen udløst af blåt lys. I dette optogenetiske system, CRY2-klynger (blå og pink) styres reversibelt af blåt lys. Hvis CRY2 er forbundet med fluorescerende proteiner (grøn -
 Nyt isoleringsmateriale giver en mere effektiv eldistributionKredit:Chalmers Tekniske Universitet Højspændings jævnstrømskabler, som effektivt kan transportere elektricitet over lange afstande, spiller en afgørende rolle i vores elforsyning. At optimere der
Nyt isoleringsmateriale giver en mere effektiv eldistributionKredit:Chalmers Tekniske Universitet Højspændings jævnstrømskabler, som effektivt kan transportere elektricitet over lange afstande, spiller en afgørende rolle i vores elforsyning. At optimere der
- Hvad er en stor teori, der forklarer, hvordan Amerika oprindeligt var befolkede?
- Maluku jordskælv:Hvorfor forårsager nogle havjordskælv tsunamier, mens andre ikke gør?
- Hvilke to tektoniske plader er adskilt af en Mid Ocean Ridge?
- Udvidelse af kraften ved attosekundspektroskopi
- Livets oprindelse i membranløse protoceller
- Radikalisering til ekstremistiske ideologier udløses ofte af negative livsbegivenheder


