Lewis Structure of Nitrogen (N₂):En trin-for-trin guide
1. Tæl valenselektroner:
* Nitrogen (N) har 5 valenselektroner.
* Da der er to nitrogenatomer, er det samlede antal valenselektroner 5 * 2 =10.
2. Forbind atomerne:
* Tegn en enkeltbinding mellem de to nitrogenatomer. Dette bruger 2 elektroner.
3. Fordel resterende elektroner:
* Du har 8 elektroner tilbage (10 - 2).
* For at opfylde oktetreglen skal du tilføje 3 ensomme par omkring hvert nitrogenatom.
4. Endelig struktur:
```
..
:N:
:N:
..
```
Nøglepunkter:
* Trippelbinding: Det diatomiske nitrogenmolekyle har en tredobbelt binding mellem nitrogenatomerne. Dette er repræsenteret af de tre linjer i strukturen.
* Oktetregel: Hvert nitrogenatom har 8 elektroner omkring sig, hvilket opfylder oktetreglen.
Lad mig vide, hvis du gerne vil se andre eksempler på Lewis-strukturer!
Sidste artikelIonisk radius:Fluor vs. Brom - Forstå atomstørrelse
Næste artikelLewis Dot Structures for O₂ og N₂:En trin-for-trin guide
 Varme artikler
Varme artikler
-
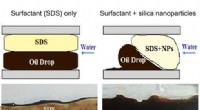 Nye materialer med vigtige anvendelser i forbedret oliegenvindingForskelle i bevægelsen af olie gennem mikrokanalerne ved tilsætning af overfladeaktivt stof i nærvær af silicananopartikler sammenlignet med det overfladeaktive middel alene, hvilket viser, hvordan
Nye materialer med vigtige anvendelser i forbedret oliegenvindingForskelle i bevægelsen af olie gennem mikrokanalerne ved tilsætning af overfladeaktivt stof i nærvær af silicananopartikler sammenlignet med det overfladeaktive middel alene, hvilket viser, hvordan -
 Hærforsker bruger matematik til at afdække ny kemiI fremtiden, materialeforskere vil bruge avanceret software til at specificere de egenskaber, de ønsker, og et program vil levere et udvalg af optimerede kemiske forbindelser. Kredit:US Army illustrat
Hærforsker bruger matematik til at afdække ny kemiI fremtiden, materialeforskere vil bruge avanceret software til at specificere de egenskaber, de ønsker, og et program vil levere et udvalg af optimerede kemiske forbindelser. Kredit:US Army illustrat -
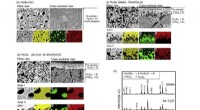 Oxidation i nyt coatingmateriale til flygasturbinemotorerOxidationsprocesserne i ytterbiumsilicid afhænger i høj grad af mængden af luft i miljøet, som vist ved scanning af elektronmikroskopibilleder og røntgendiffraktionstoppe. Kredit:Ryo Inoue fra Tokyo
Oxidation i nyt coatingmateriale til flygasturbinemotorerOxidationsprocesserne i ytterbiumsilicid afhænger i høj grad af mængden af luft i miljøet, som vist ved scanning af elektronmikroskopibilleder og røntgendiffraktionstoppe. Kredit:Ryo Inoue fra Tokyo -
 3-D bioprint af levende strukturer med indbyggede kemiske sensorer3D bioprintet struktur indeholdende grønne alger (Chlamydomonas) i en hydrogel. Kredit:Anja Lode, TU Dresden En ny metode muliggør ikke-invasiv overvågning af iltmetabolisme i celler, der er 3-D b
3-D bioprint af levende strukturer med indbyggede kemiske sensorer3D bioprintet struktur indeholdende grønne alger (Chlamydomonas) i en hydrogel. Kredit:Anja Lode, TU Dresden En ny metode muliggør ikke-invasiv overvågning af iltmetabolisme i celler, der er 3-D b
- Hvordan kan brint opnås?
- Klima forandring, vand og spredning af sygdomme:Forbind prikkerne forskelligt
- Hvad er fakta om den voksende halvmåne?
- UV smalbånds fotodetektor baseret på indiumoxid nanokrystaller
- Beskriv de typer energi, der genereres, når du rammer en søm med hammer?
- Hvad er den mest almindelige utilsigtede energitransformation?


