Ionisk radius:Fluor vs. Brom - Forstå atomstørrelse
* Atomstørrelse: Brom er placeret under Fluor i det periodiske system, hvilket betyder, at det har en ekstra elektronskal. Dette gør brom i sagens natur større end fluor.
* Effektiv nuklear ladning: Mens begge grundstoffer har en større positiv ladning i deres ioniske tilstand (de får en elektron til at blive anioner), beskytter den ekstra elektronskal i brom effektivt de ydre elektroner fra kernen. Dette svækker tiltrækningen mellem kernen og de ydre elektroner, hvilket fører til en større ionradius.
Opsummering: Når du bevæger dig ned ad en gruppe i det periodiske system, øges atom- og ionradius på grund af tilføjelsen af elektronskaller og den aftagende virkning af kerneladning på de yderste elektroner.
 Varme artikler
Varme artikler
-
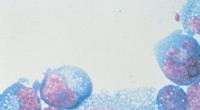 Hvordan fosfat- og bikarbonatbuffere holder vores kroppe i balanceAf Marie‑Luise Blue, Opdateret 24. marts 2022 Hvad er pH? pH-skalaen kvantificerer surheden eller alkaliniteten af en opløsning ved at måle logaritmen af hydrogenionkoncentrationen. En højere koncent
Hvordan fosfat- og bikarbonatbuffere holder vores kroppe i balanceAf Marie‑Luise Blue, Opdateret 24. marts 2022 Hvad er pH? pH-skalaen kvantificerer surheden eller alkaliniteten af en opløsning ved at måle logaritmen af hydrogenionkoncentrationen. En højere koncent -
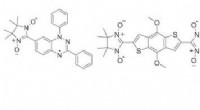 Overvindelse af udfordringerne med kontrolleret termisk aflejring af organiske diradikale stofferVenstre panel:Diradikalerne undersøgt i dette arbejde. Højre panel:Skitse af forskellige film (grøn farve) afsat på et underlag (grå farve). Kredit:Tuebingen Universitet Magnetisme er en egenskab
Overvindelse af udfordringerne med kontrolleret termisk aflejring af organiske diradikale stofferVenstre panel:Diradikalerne undersøgt i dette arbejde. Højre panel:Skitse af forskellige film (grøn farve) afsat på et underlag (grå farve). Kredit:Tuebingen Universitet Magnetisme er en egenskab -
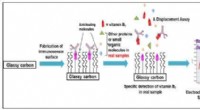 B7 -vitaminovervågningsenhed til analyse af fødevarer og kliniske prøverUdvikling af en elektrokemisk immunosensor til direkte påvisning af vitamin B7 i rigtige prøver. Kredit:Dr. Khor Sook Mei Direkte påvisning af vitamin B7 i ægte prøve er mulig ved hjælp af den udv
B7 -vitaminovervågningsenhed til analyse af fødevarer og kliniske prøverUdvikling af en elektrokemisk immunosensor til direkte påvisning af vitamin B7 i rigtige prøver. Kredit:Dr. Khor Sook Mei Direkte påvisning af vitamin B7 i ægte prøve er mulig ved hjælp af den udv -
 Bæredygtige 3D-printede supermagneterPå Graz teknologiske universitet, miniaturiserede supermagneter blev produceret for første gang ved hjælp af laserbaseret 3D-print. Kredit:IMAT – TU Graz Fra vindmøller og elektriske motorer til s
Bæredygtige 3D-printede supermagneterPå Graz teknologiske universitet, miniaturiserede supermagneter blev produceret for første gang ved hjælp af laserbaseret 3D-print. Kredit:IMAT – TU Graz Fra vindmøller og elektriske motorer til s
- Hvordan dannes spiralgalakser, og hvilke processer bidrager til deres unikke struktur?
- Hvilke måder samarbejder organismer med hinanden for at sikre stabiliteten i deres økosystem?
- Hvad er en stor masse faldet klippe?
- Udbredt forbrug af flodhestetænder kombineret med ufuldstændige handelsregistre bringer truede flo…
- Wendelstein 7-X konceptet beviser sin effektivitet
- Hvorfor det føles så godt at være bange


