Hvordan fosfat- og bikarbonatbuffere holder vores kroppe i balance
Af Marie‑Luise Blue, Opdateret 24. marts 2022
Hvad er pH?
pH-skalaen kvantificerer surheden eller alkaliniteten af en opløsning ved at måle logaritmen af hydrogenionkoncentrationen. En højere koncentration af H⁺-ioner sænker pH, mens en lavere koncentration hæver den. På en skala fra 0 til 14 angiver en pH-værdi på 7 neutralitet, værdier under 7 er sure, og værdier over 7 er alkaliske.
Sådan fungerer buffere
Buffere stabiliserer pH ved at balancere en svag syre og dens konjugerede svage base. Når overskydende H⁺-ioner opstår, sekvestrerer den svage base dem, omdannes til dens sure form og opretholder pH. Omvendt, når en base tilsættes, donerer den svage syre H⁺-ioner og skifter tilbage mod neutralitet.
Fosfatbuffersystemet
Inde i cellerne holder fosfatbufferen – omfattende dihydrogenphosphat (H₂PO₄⁻) og hydrogenphosphat (HPO₄²⁻) – den intracellulære pH-værdi tæt på fysiologiske værdier. Med en dissociationskonstant (pKa) på 7,21 er ligevægten af dette par tæt på linje med den typiske cytosoliske pH på 7,2-7,4, hvilket gør det yderst effektivt til intracellulær homeostase (standard biokemiske referencer).
Når fosfatbuffersystemet er utilstrækkeligt
I kredsløbssystemet kan de begrænsede koncentrationer af dihydrogen og hydrogenphosphat ikke buffere blod effektivt. Her opretholder bicarbonatbufferen - dannet af opløst CO₂ som bicarbonat (HCO₃⁻) og kulsyre (H₂CO₃) - blodets pH på cirka 7,4. Åndedrætsudånding af CO₂ fjerner overskydende kulsyre, hvilket tillader bikarbonatsystemet at fungere effektivt.
 Varme artikler
Varme artikler
-
 Vi har opdaget en måde at genvinde DNA fra fingeraftryk uden at ødelægge demKredit:Shutterstock Fingeraftryk indeholder meget mere information, end du måske er klar over. De giver ikke kun et mønster, som man kan identificere folk med. De kan også indeholde DNA. Og da hve
Vi har opdaget en måde at genvinde DNA fra fingeraftryk uden at ødelægge demKredit:Shutterstock Fingeraftryk indeholder meget mere information, end du måske er klar over. De giver ikke kun et mønster, som man kan identificere folk med. De kan også indeholde DNA. Og da hve -
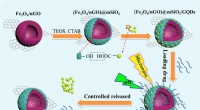 N-dopede carbonindkapslede overgangsmetalkatalysatorer for at optimere ydeevnen af zink-luftbatter…Fe@NCG blev fremstillet ved pyrolysering af opløsningsmiddelfri dannede Fechitosan-chelater og yderligere nitrogen-urinstof med lille molekyle. Den dannede katalysator udviser bifunktionel katalytisk
N-dopede carbonindkapslede overgangsmetalkatalysatorer for at optimere ydeevnen af zink-luftbatter…Fe@NCG blev fremstillet ved pyrolysering af opløsningsmiddelfri dannede Fechitosan-chelater og yderligere nitrogen-urinstof med lille molekyle. Den dannede katalysator udviser bifunktionel katalytisk -
 Røntgenforsøg bidrager til undersøgelser af et lægemiddel, der nu er godkendt til at bekæmpe tu…En Pretomanid pille. Lægemidlet blev udviklet af nonprofit TB Alliance. Kredit:TB Alliance U.S. Food and Drug Administration har godkendt et nyt antibiotikum, i kombination med to eksisterende ant
Røntgenforsøg bidrager til undersøgelser af et lægemiddel, der nu er godkendt til at bekæmpe tu…En Pretomanid pille. Lægemidlet blev udviklet af nonprofit TB Alliance. Kredit:TB Alliance U.S. Food and Drug Administration har godkendt et nyt antibiotikum, i kombination med to eksisterende ant -
 Dalian kohærent lyskilde afslører iltproduktion fra tre-legeme fotodissociation af vandDalian Coherent Light Source afslører tre-legeme fotodissociation af vand som en vigtig præbiotisk-O2 kilde. Kredit:DICP Herkomsten af ilt på Jorden og andre solar planetariske legemer er et gru
Dalian kohærent lyskilde afslører iltproduktion fra tre-legeme fotodissociation af vandDalian Coherent Light Source afslører tre-legeme fotodissociation af vand som en vigtig præbiotisk-O2 kilde. Kredit:DICP Herkomsten af ilt på Jorden og andre solar planetariske legemer er et gru
- Hvorfor er kogepunktet for H2O meget højere end h2se?
- Er der virkelig en 1 ud af 6 chance for menneskelig udryddelse i dette århundrede?
- Må skoven være med dig:GEDI bevæger sig mod opsendelse til rumstation
- Hvordan indstiller du tid og dato på et Aqua Starz solcelledrevet ur?
- Hvordan vil du definere energimåler konstant?
- Hvorfor er hydrogenbinding kun mulig med brint?


