Hvorfor er hydrogenbinding kun mulig med brint?
Her er grunden til, at det er specifikt stærkt med disse elementer:
* Høj elektronegativitet: Oxygen, fluor og nitrogen er meget elektronegative, hvilket betyder, at de trækker elektroner mod sig selv i en binding. Dette skaber en stærk delvis negativ ladning (Δ-) på det elektronegative atom og en stærk delvis positiv ladning (δ+) på hydrogenatomet.
* lille størrelse: Disse elektronegative atomer er små, hvilket gør det muligt for hydrogenatomet at komme tæt nok på de ensomme par elektroner på det elektronegative atom, hvilket danner en stærk dipol-dipol-interaktion.
Hvorfor andre elementer ikke danner brintbindinger:
* lavere elektronegativitet: Andre elementer, som kulstof eller klor, har lavere elektronegativitet end ilt, fluor eller nitrogen. Dette resulterer i svagere delvise ladninger, hvilket fører til svagere dipol-dipol-interaktioner.
* Større størrelse: Større atomer er mindre tilbøjelige til at danne stærke brintbindinger, fordi brintatomet ikke kan komme tæt nok på de ensomme parelektroner.
Derfor er hydrogenbinding en specifik type interaktion, der involverer brint og stærkt elektronegative atomer som ilt, fluor eller nitrogen. Det er ikke begrænset til brint.
Sidste artikelHvorfor har calciumcarbonat brug for en høj temperatur for at nedbrydes?
Næste artikelHvilke typer obligationer danner vand?
 Varme artikler
Varme artikler
-
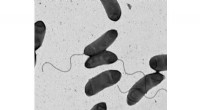 En usædvanlig form for antibiotikaresistens ved pandemisk koleraBilledet er et elektronmikrografi af bakterien Vibrio kolerae , det forårsagende middel til koleraen. Kredit:M. Stephen Trent, University of Georgia Kolera er en ødelæggende sygdom for millioner
En usædvanlig form for antibiotikaresistens ved pandemisk koleraBilledet er et elektronmikrografi af bakterien Vibrio kolerae , det forårsagende middel til koleraen. Kredit:M. Stephen Trent, University of Georgia Kolera er en ødelæggende sygdom for millioner -
 Sammensætning af multikomponentlegeringer ved screening med høj gennemstrømningFigur 1:(a) Skematisk diagram over høj gennemløb, (b) fysisk skygge maske. Kredit:© Science China Press Multikomponentmaterialer er blandt de mest lovende materialer inden for teknik og biomedicin
Sammensætning af multikomponentlegeringer ved screening med høj gennemstrømningFigur 1:(a) Skematisk diagram over høj gennemløb, (b) fysisk skygge maske. Kredit:© Science China Press Multikomponentmaterialer er blandt de mest lovende materialer inden for teknik og biomedicin -
 En naturinspireret belægning for at forhindre, at stoffer nedbrydes for tidligtForskere har udviklet en tynd belægning, der kan gøre det muligt for medicin at have færre tilsætningsstoffer. Kredit:Shutterstock.com Kemikere har udviklet en belægning, der kan gøre visse lægemi
En naturinspireret belægning for at forhindre, at stoffer nedbrydes for tidligtForskere har udviklet en tynd belægning, der kan gøre det muligt for medicin at have færre tilsætningsstoffer. Kredit:Shutterstock.com Kemikere har udviklet en belægning, der kan gøre visse lægemi -
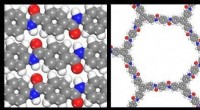 Samarbejde fører til 2-D polymer opdagelseKredit:The Army Research Laboratory Hærens forskere nåede et gennembrud i den begyndende videnskab om todimensionelle polymerer takket være et samarbejdsprogram, der får hjælp fra ledende videnska
Samarbejde fører til 2-D polymer opdagelseKredit:The Army Research Laboratory Hærens forskere nåede et gennembrud i den begyndende videnskab om todimensionelle polymerer takket være et samarbejdsprogram, der får hjælp fra ledende videnska
- Hvad er den ioniske ligning for HCL CH3NH2?
- Kunstige gletsjere som reaktion på klimaændringer?
- Fem års resultater antyder Australiens fremtidige reaktion på vores skiftende atmosfære
- Antitrustregulatorer kaster sig over Big Tech, når sonderne udvides
- Regulering af todimensionelle nanomaterialer til lithium-ion-batterier
- Hvilke kemiske reaktioner er den type kemikalier, der brydes,?


