Hvorfor har calciumcarbonat brug for en høj temperatur for at nedbrydes?
* Stærke obligationer: Bindingerne mellem calcium, kulstof og ilt i calciumcarbonat er ret stærke. Disse obligationer kræver en betydelig mængde energi for at bryde.
* Nedbrydningsprodukter: Nedbrydningen af calciumcarbonat producerer calciumoxid (CAO) og kuldioxid (CO2). Dette er en kemisk ændring, hvor det originale molekyle opdeles i enklere molekyler.
* Energiindgang: Den energi, der er nødvendig for at bryde disse bindinger, kommer fra varmen. Jo højere temperatur, jo mere kinetisk energi har molekylerne, hvilket øger sandsynligheden for binding af binding.
Kort sagt kræver den høje aktiveringsenergi, der er nødvendig for at bryde de stærke bindinger i calciumcarbonat, en høj temperatur for at starte nedbrydningsreaktionen.
Her er reaktionen:
CACO3 (S) + varme → Cao (S) + CO2 (G)
Bemærk: Nedbrydningen af calciumcarbonat er en reversibel reaktion. Ved lavere temperaturer favoriseres den omvendte reaktion (reaktionen af calciumoxid med kuldioxid til dannelse af calciumcarbonat).
 Varme artikler
Varme artikler
-
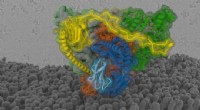 Informationsfilter til immunforsvarStruktur af MHC-I peptid-belastningskomplekset i membranen af det endoplasmatiske reticulum. Kredit:S. Trowitzsch, A. Möller, R. Tampé I dag, sociale medier hjælper os med at holde os ajour med
Informationsfilter til immunforsvarStruktur af MHC-I peptid-belastningskomplekset i membranen af det endoplasmatiske reticulum. Kredit:S. Trowitzsch, A. Möller, R. Tampé I dag, sociale medier hjælper os med at holde os ajour med -
 Mærkelige ting sker, når en krystal er delt i toEn labyrintlignende struktur opstår på overfladen. Kredit:TU Wien Den bemærkelsesværdige styrke af ioniske krystaller er let forklaret på atomær skala:Positivt og negativt ladede atomer sidder sid
Mærkelige ting sker, når en krystal er delt i toEn labyrintlignende struktur opstår på overfladen. Kredit:TU Wien Den bemærkelsesværdige styrke af ioniske krystaller er let forklaret på atomær skala:Positivt og negativt ladede atomer sidder sid -
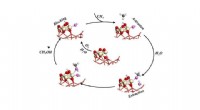 Vand er nøglen til katalytisk omdannelse af methan til methanolKatalytisk cyklus til selektiv omdannelse af methan til methanol ved at udsætte metanen for ilt og vand. Kredit:Brookhaven National Laboratory Forskere ved det amerikanske energiministerium Brookh
Vand er nøglen til katalytisk omdannelse af methan til methanolKatalytisk cyklus til selektiv omdannelse af methan til methanol ved at udsætte metanen for ilt og vand. Kredit:Brookhaven National Laboratory Forskere ved det amerikanske energiministerium Brookh -
 Duften af klæbemidlerForskerne i Freising stoler på en række forskellige analysemetoder, inklusive gaskromatografi, at opdage årsagerne til ubehagelige lugte i akrylklæbemidler. Kredit:Fraunhofer-Gesellschaft Det er e
Duften af klæbemidlerForskerne i Freising stoler på en række forskellige analysemetoder, inklusive gaskromatografi, at opdage årsagerne til ubehagelige lugte i akrylklæbemidler. Kredit:Fraunhofer-Gesellschaft Det er e


