Hvad er den ioniske ligning for HCL CH3NH2?
1. Reaktionen:
HCL (aq) + CH3NH2 (aq) → CH3NH3 + (aq) + Cl- (aq)
Dette repræsenterer reaktionen af saltsyre (HCI) med methylamin (CH3NH2) til dannelse af methylammoniumion (CH3NH3+) og chloridion (Cl-).
2. Identificering af stærke elektrolytter:
* hcl er en stærk syre, så den ioniserer fuldstændigt i opløsningen.
* CH3NH2 er en svag base, hvilket betyder, at den kun delvist ioniserer i opløsningen.
* CH3NH3+ er en svag konjugatsyre og eksisterer for det meste som ioner.
* cl- er en tilskuerion (den deltager ikke i reaktionen).
3. Den komplette ioniske ligning:
H + (aq) + Cl- (aq) + CH3NH2 (aq) → CH3NH3 + (aq) + Cl- (aq)
4. Den nettoioniske ligning:
H+ (aq)+ CH3NH2 (aq) → CH3NH3+ (aq)
Forklaring:
* Den nettoioniske ligning viser kun de arter, der er direkte involveret i reaktionen.
* Chloridionerne (Cl-) er tilskuerioner, hvilket betyder, at de vises på begge sider af ligningen og ændrer sig ikke.
* Denne ligning repræsenterer protonationen af methylamin med hydrogenioner (H+) til dannelse af methylammoniumion (CH3NH3+).
Nøglepunkt: Den nettoioniske ligning er den mest nyttige form for ligningen, da den fremhæver den faktiske kemiske ændring, der forekommer.
 Varme artikler
Varme artikler
-
 En rekordlang polymer DNA negativPå Institut for Fysisk Kemi ved Det Polske Videnskabsakademi i Warszawa blev et rekordlangt fragment af DNA indprentet i polymeren. Kredit:IPC PAS, Grzegorz Krzyzewski Et fragment af en enkelt DNA
En rekordlang polymer DNA negativPå Institut for Fysisk Kemi ved Det Polske Videnskabsakademi i Warszawa blev et rekordlangt fragment af DNA indprentet i polymeren. Kredit:IPC PAS, Grzegorz Krzyzewski Et fragment af en enkelt DNA -
 At sikre oral medicin er beskyttet mod de sure tilstande i mavenKredit:Shutterstock En gruppe af kemiske og biomedicinske ingeniører ved UNSW Sydney og University of Cambridge har forbedret den kemiske stabilitet af ZIF-krystaller, gør det muligt at bruge diss
At sikre oral medicin er beskyttet mod de sure tilstande i mavenKredit:Shutterstock En gruppe af kemiske og biomedicinske ingeniører ved UNSW Sydney og University of Cambridge har forbedret den kemiske stabilitet af ZIF-krystaller, gør det muligt at bruge diss -
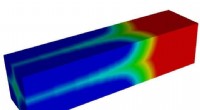 Undersøgelse afslører ukendte detaljer om almindelige lithium-ion batterimaterialerEn illustration viser væksten af en lithium-mangel fase (blå) på bekostning af en lithium-rig fase (rød) i en lithium jernfosfat mikrostav. Rice University-forskere ledede en undersøgelse, der fandt
Undersøgelse afslører ukendte detaljer om almindelige lithium-ion batterimaterialerEn illustration viser væksten af en lithium-mangel fase (blå) på bekostning af en lithium-rig fase (rød) i en lithium jernfosfat mikrostav. Rice University-forskere ledede en undersøgelse, der fandt -
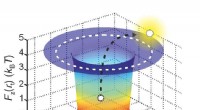 Den første præcise måling af et enkelt molekyls effektive ladningForskere kan bestemme den effektive elektriske ladning af et molekyle ved at fange det i en potentiel brønd ved at måle, hvor længe det bliver inde. Kredit:Madhavi Krishnan / University of Zurich
Den første præcise måling af et enkelt molekyls effektive ladningForskere kan bestemme den effektive elektriske ladning af et molekyle ved at fange det i en potentiel brønd ved at måle, hvor længe det bliver inde. Kredit:Madhavi Krishnan / University of Zurich
- Sådan konverteres en skrå højde til en normal højde
- Hvordan bruger du en som adjektiv i en sætning?
- Hvad er betydningen af nukleinsyrer?
- Hvad holder DNA'et i en eukaryotisk celle?
- Med malede ansigter, kunstnere kæmper mod ansigtsgenkendelsesteknologi
- Undersøgelse undersøger omkostningerne ved at lukke atomkraftværker i Tyskland


