Den første præcise måling af et enkelt molekyls effektive ladning
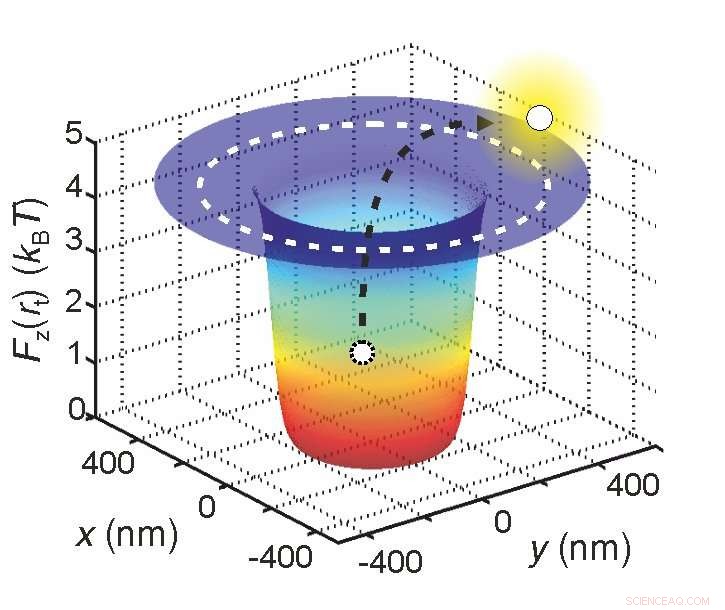
Forskere kan bestemme den effektive elektriske ladning af et molekyle ved at fange det i en potentiel brønd ved at måle, hvor længe det bliver inde. Kredit:Madhavi Krishnan / University of Zurich
For første gang, forskere har præcist målt den effektive elektriske ladning af et enkelt molekyle i opløsning. Denne grundlæggende indsigt fra en SNSF-professor kunne også bane vejen for fremtidig medicinsk diagnostik.
Elektrisk ladning er en af de nøgleegenskaber, der tillader molekyler at interagere. Selve livet afhænger af dette fænomen:mange biologiske processer involverer interaktioner mellem molekyler som proteiner, hvor deres afgift spiller en væsentlig rolle. Endnu, ladningen af et protein i et vandigt miljø - dets naturlige kontekst i en levende organisme - er svær at bestemme præcist ved hjælp af traditionelle metoder.
Madhavi Krishnan, som har et SNSF professorat ved universitetet i Zürich, har udviklet en metode til præcist at måle ladningen af et enkelt molekyle i opløsning. Hendes fremmarch blev beskrevet i en række artikler i Natur nanoteknologi , Fysisk gennemgang E og Journal of Chemical Physics . Denne opdagelse kunne bane vejen for nye diagnostiske værktøjer siden, på et kemisk niveau, mange sygdomme er forbundet med et skift i et proteins elektriske ladning, som forhindrer molekylet i at virke, som det skal.
Et molekyles elektriske ladning kan være ret forskellig i gasfasen og i opløsning. Årsagen til denne forskel ligger i komplekse interaktioner mellem objektet og den omgivende væske. Derfor, standard gasfasemålinger giver ikke direkte information om molekylets adfærd i dets biologiske kontekst.
"Som børn sparker en bold"
Molekyler i opløsning er i konstant bevægelse, tilfældigt sparker hinanden. Krishnan og Ph.D. studerende Francesca Ruggeri udnyttede dette velkendte fænomen, kaldet Brownsk bevægelse, for at måle den effektive ladning af et molekyle direkte i opløsning.
Først, de fangede molekylet i en "potentiel brønd". I stedet for en egentlig brønd, dette er en situation, hvor den potentielle energi af molekylet er på sit minimum. I en sådan situation, hoppende vandmolekyler forsøger kontinuerligt at uddrive molekylet fra brønden.
"Det er som børn, der leger med en bold i bunden af en pit, " forklarer Krishnan. "Kuglen er det molekyle, vi er interesserede i, og børnene er vandmolekylerne. Bolden skulle have et ret hårdt spark for at kunne flyve ud af pit."
Jo højere den effektive ladning af molekylet, jo større dybden af den potentielle brønd og, følgelig, jo lavere er sandsynligheden for, at molekylet skubbes ud fra brønden. I praksis, det betyder, at den tid, det tager for molekylet at blive sparket ud af brønden, er direkte relateret til dets effektive ladning.
"I sidste ende koger det ned til et statistisk princip, " forklarer Krishnan. "Hvis vi ved, hvor længe et molekyle forbliver fanget i brønden, vi ved præcis, hvor dyb brønden er. Og da denne dybde afhænger direkte af molekylets effektive ladning, vi kan også udlede denne værdi meget præcist."
To glasplader
For at skabe en potentiel brønd, videnskabsmænd komprimerede en opløsning indeholdende proteinerne mellem to glasplader, en af dem er dækket af mikroskopiske huller. Molekyler fanget i potentielle brønde blev mærket med fluorescerende midler, hvilket gjorde det muligt at spore dem med et optisk mikroskop.
Selvom opdagelsen har vigtige grundlæggende konsekvenser, det kunne også bane vejen for nye diagnostiske værktøjer til mange sygdomme forårsaget af fejlformede proteiner, såsom Alzheimers og kræft. "Vi ved, at 3D-konformationen af et protein påvirker dets effektive ladning, og vores arbejde kan præsentere en ny vej til at opdage defekte proteiner."
Sidste artikelVedligeholdelse af rapsoliekvalitet
Næste artikelSubtile ændringer i kemisk struktur kan påvirke lægemiddeltoksicitet
 Varme artikler
Varme artikler
-
 "How to Calculate Heat Flux, 3, [[ Varmeflux eller varmeoverførsel pr. hastighedsenhedsareal er en nyttig mængde i applikationer såsom bestemmelse af overførsel af energi fra en brændstofplade til arbejdsvæske, såsom i en
"How to Calculate Heat Flux, 3, [[ Varmeflux eller varmeoverførsel pr. hastighedsenhedsareal er en nyttig mængde i applikationer såsom bestemmelse af overførsel af energi fra en brændstofplade til arbejdsvæske, såsom i en -
 Synkrotronundersøgelse afslører oxygens indflydelse på kemien af atmosfærisk forureningEt repræsentativt brændstofmolekyle, der viser iltmolekyler (højre, rød) og 2-methylheptan (højre, grå og hvid) mødes i en jet-omrørt reaktor. De stærkt oxygenerede molekyler, der resulterer (til vens
Synkrotronundersøgelse afslører oxygens indflydelse på kemien af atmosfærisk forureningEt repræsentativt brændstofmolekyle, der viser iltmolekyler (højre, rød) og 2-methylheptan (højre, grå og hvid) mødes i en jet-omrørt reaktor. De stærkt oxygenerede molekyler, der resulterer (til vens -
 Massespektrometrisk billeddannelsesteknik gør diagnosticering nemmere og smartereHøj opløsning atmosfærisk tryk massespektrometri billeddannelsessystem. Kredit:Daegu Gyeongbuk Institut for Videnskab og Teknologi (DGIST) Et forskerhold ved DGIST har for nylig udviklet en teknol
Massespektrometrisk billeddannelsesteknik gør diagnosticering nemmere og smartereHøj opløsning atmosfærisk tryk massespektrometri billeddannelsessystem. Kredit:Daegu Gyeongbuk Institut for Videnskab og Teknologi (DGIST) Et forskerhold ved DGIST har for nylig udviklet en teknol -
 Video:Sådan interagerer du akavet med mennesker på en bar ved hjælp af kemiKredit:The American Chemical Society Med pandemiske restriktioner ophævet i USA, vi begynder at komme tilbage i verden, mødes med venner og kolleger på restauranter og barer. Hvis du er bekymret,
Video:Sådan interagerer du akavet med mennesker på en bar ved hjælp af kemiKredit:The American Chemical Society Med pandemiske restriktioner ophævet i USA, vi begynder at komme tilbage i verden, mødes med venner og kolleger på restauranter og barer. Hvis du er bekymret,


