Hydrogenchloridreaktioner:Hydrolyse og interaktion med methylbenzen
1. Reaktion med vand:
* HCl er en stærk syre. Når det tilsættes til vand, ioniseres det fuldstændigt, hvilket betyder, at det opdeles i hydrogenioner (H+) og chloridioner (Cl-):
```
HCl (g) + H2O (l) → H3O+ (vandig) + Cl- (vandig)
```
* H+-ionerne reagerer med vandmolekyler og danner hydroniumioner (H3O+).
* Opløsningen bliver sur. Tilstedeværelsen af H3O+ ioner gør opløsningen sur.
2. Interaktion med methylbenzen:
* Methylbenzen (toluen) er en ikke-polær organisk forbindelse. Det opløses ikke let i vand, som er et polært opløsningsmiddel.
* HCl reagerer ikke direkte med methylbenzen. Mens HCl er surt, har det ikke en stærk nok affinitet til, at den aromatiske ring i toluen kan forårsage en signifikant reaktion.
* HCl kan dog opløses lidt i methylbenzen. Dette skyldes svage interaktioner mellem det polære HCl-molekyle og elektronskyen i benzenringen.
Samlet set:
Når du tilføjer HCl til en blanding af vand og methylbenzen, vil følgende ske:
* HCI'en vil primært opløses i vandet og ionisere og danne en sur opløsning.
* Der vil være en meget lille mængde HCl, der opløses i methylbenzen.
* Methylbenzen- og vandlagene vil sandsynligvis adskilles, hvor methylbenzenlaget (toluen) flyder oven på vandet.
Vigtig bemærkning: Den faktiske mængde HCl, der opløses i methylbenzenlaget, vil være meget lille i forhold til den mængde, der opløses i vandlaget. Dette skyldes den betydelige forskel i polaritet mellem de to opløsningsmidler.
 Varme artikler
Varme artikler
-
 Sådan bygger du effektive organiske solcellerFeng Gao, lektor ved Linköpings Universitet, Sverige. Kredit:Göran Billeson Organiske solceller, lavet af kulstofbaserede materialer, frembyder unikke fordele sammenlignet med andre solcelleteknol
Sådan bygger du effektive organiske solcellerFeng Gao, lektor ved Linköpings Universitet, Sverige. Kredit:Göran Billeson Organiske solceller, lavet af kulstofbaserede materialer, frembyder unikke fordele sammenlignet med andre solcelleteknol -
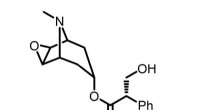 Forskere rapporterer fuldt syntetisk vej til scopolamin, anti-kvalmemiddelSwRI udvikler omkostningseffektive metoder til at syntetisere nye formuleringer til plantebaserede lægemidler, senest en syntetisk version af en populær behandling mod kvalme. Kredit:Southwest Researc
Forskere rapporterer fuldt syntetisk vej til scopolamin, anti-kvalmemiddelSwRI udvikler omkostningseffektive metoder til at syntetisere nye formuleringer til plantebaserede lægemidler, senest en syntetisk version af en populær behandling mod kvalme. Kredit:Southwest Researc -
 En bioplast afledt af sojaprotein, som kan absorbere op til 40 gange sin egen vægtDette nye produkt, som er organisk og biologisk nedbrydeligt, er miljøvenlig. Af den grund, eksperterne undersøger brugen af det inden for havebrug, specifikt som et råmateriale til fremstilling af
En bioplast afledt af sojaprotein, som kan absorbere op til 40 gange sin egen vægtDette nye produkt, som er organisk og biologisk nedbrydeligt, er miljøvenlig. Af den grund, eksperterne undersøger brugen af det inden for havebrug, specifikt som et råmateriale til fremstilling af -
 Er det muligt at udvikle antiaromaticitet af ikke-benzenoide aromatiske forbindelser?Er det muligt at udvikle antiaromaticitet af ikke-benzenoide aromatiske forbindelser? Kredit:Graduate School of Science and Engineering, Ehime University Cirkulært konjugerede forbindelser med s er
Er det muligt at udvikle antiaromaticitet af ikke-benzenoide aromatiske forbindelser?Er det muligt at udvikle antiaromaticitet af ikke-benzenoide aromatiske forbindelser? Kredit:Graduate School of Science and Engineering, Ehime University Cirkulært konjugerede forbindelser med s er
- Hvorfor akkumuleres ikke sedimenter overalt?
- Mitose vs. Meiose:Nøgleligheder, forskelle og deres roller i livet
- Forståelse af luft:hvorfor det er en blanding, ikke en løsning
- Hvor finder du variation inden for en art?
- Gengiver plante deres egen art?
- Hvad gør Alka Seltzer for at vandes, når den blandes med olie?


