Kovalente bindinger:Forståelse af elektrondeling og oktetreglen
Her er hvorfor:
* Valenselektroner: Det er elektronerne i den yderste skal af et atom, som er involveret i kemisk binding.
* Oktetregel: Hovedgruppeelementer har tendens til at vinde, miste eller dele elektroner for at opnå en stabil elektronkonfiguration med otte valenselektroner (som en ædelgas).
* Kovalent binding: Atomer deler elektroner for at opnå denne stabile konfiguration.
Eksempel:
Overvej iltmolekylet (O2). Hvert oxygenatom har seks valenselektroner. For at opnå en oktet deler hvert oxygenatom to af dets elektroner med det andet oxygenatom. Dette resulterer i en dobbeltbinding med i alt fire delte elektroner (to fra hvert atom).
Selvom det er muligt for atomer at dele mere end otte elektroner i nogle tilfælde (især med overgangsmetaller), er dette ikke almindeligt for hovedgruppeelementer.
Sidste artikelAntal elektroner i en chlorion:Forståelse af Cl⁻
Næste artikelUdfældningsreaktioner:Definition, forklaring og eksempler
 Varme artikler
Varme artikler
-
 Forskere rekrutterer nye atomare sværvægtere i målrettet kamp mod kræftKatherine Shield (fra venstre), Dahlia An, Tyler Bailey på Lawrence Berkeley National Laboratory tirsdag, 17. november kl. 2020, i Berkeley, Californien Kredit:Marilyn Sargent/Berkeley Lab En love
Forskere rekrutterer nye atomare sværvægtere i målrettet kamp mod kræftKatherine Shield (fra venstre), Dahlia An, Tyler Bailey på Lawrence Berkeley National Laboratory tirsdag, 17. november kl. 2020, i Berkeley, Californien Kredit:Marilyn Sargent/Berkeley Lab En love -
 Avancerede biomaterialer med silkefibroin-bioaktivt glas til at konstruere patientspecifikke 3D-knog…Udvikling af avancerede hybride biomaterialer ved hjælp af tilpasset 3D-printsoftware. Kredit:RoboCAD, 3D blæk, LLC, doi:10.1088/1748-605X/aad2a9 Den komplekse arkitektur af knogler er udfordrende
Avancerede biomaterialer med silkefibroin-bioaktivt glas til at konstruere patientspecifikke 3D-knog…Udvikling af avancerede hybride biomaterialer ved hjælp af tilpasset 3D-printsoftware. Kredit:RoboCAD, 3D blæk, LLC, doi:10.1088/1748-605X/aad2a9 Den komplekse arkitektur af knogler er udfordrende -
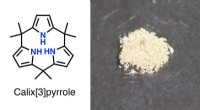 Pyrrolkemi:Gode ting kommer i treDen kemiske struktur og faststofkrystaller af calix[3]pyrrol. Kredit:Inokuma Laboratory En ny tilgang fører til den længe ventede dannelse af ringe lavet af tre pyrroler, som kunne bruges til at f
Pyrrolkemi:Gode ting kommer i treDen kemiske struktur og faststofkrystaller af calix[3]pyrrol. Kredit:Inokuma Laboratory En ny tilgang fører til den længe ventede dannelse af ringe lavet af tre pyrroler, som kunne bruges til at f -
 Kunstige bier fra en trykkoger?Ola Gjønnes Grendal bruger en metode, der fungerer som en trykkoger, til at skabe et materiale, der kan forvandles til kunstige bier. Kredit:Karoline Ravndal Lorentzen, NTNU Hvad hvis vi kunne ska
Kunstige bier fra en trykkoger?Ola Gjønnes Grendal bruger en metode, der fungerer som en trykkoger, til at skabe et materiale, der kan forvandles til kunstige bier. Kredit:Karoline Ravndal Lorentzen, NTNU Hvad hvis vi kunne ska
- Hvad sker der med den kinetiske energi, når et stof afkøles?
- Hvorfor kan en shaken sodavand eksplodere på havbunden?
- Et indfødt træ kaldte undertiden vandfaldstræet?
- Forskere demonstrerer modulering af infrarødt lys med grafen
- Fakta om det gamle egyptiske Nildelta-område
- En enkelt dosis urinstofdrevne nanorobotter reducerer blæretumorer med 90 % i museundersøgelse


