Natriumchloriddannelse:Forståelse af den ioniske binding
1. Elektronisk konfiguration:
* Natrium har en elektron i sin yderste skal (valenselektron).
* Klor har syv elektroner i sin yderste skal.
2. Stabilitetsdrevet:
* Atomer stræber efter en fuld ydre skal af elektroner for stabilitet. Dette er grundlaget for oktetreglen (bortset fra brint og helium, som sigter mod en duet, hvilket betyder to elektroner i deres ydre skal).
3. Overførsel af elektroner:
* Natrium mister let sin enkeltvalenselektron for at blive en positivt ladet ion (Na+).
* Klor får let en elektron til at fylde sin ydre skal og bliver til en negativt ladet ion (Cl-).
4. Elektrostatisk tiltrækning:
* De modsat ladede natrium- og chloridioner tiltrækker hinanden på grund af elektrostatiske kræfter og danner en ionbinding. Denne tiltrækning holder ionerne sammen i en krystalgitterstruktur.
5. Dannelse af natriumchlorid (NaCl):
* Den stærke elektrostatiske tiltrækning mellem Na+ og Cl-ioner resulterer i dannelsen af natriumchlorid (NaCl), en neutral forbindelse.
Opsummering: Natrium danner en ionbinding med klor ved at donere sin valenselektron til klor, hvilket resulterer i dannelsen af stabile ioner, der tiltrækker hinanden på grund af deres modsatte ladninger. Denne tiltrækning fører til dannelsen af natriumchlorid (NaCl).
Sidste artikelTums:Er de sure eller alkaliske? Forståelse af antacida
Næste artikelBeregning af hydrogenkrav til kulstof-nitrogenmolekyler
 Varme artikler
Varme artikler
-
 Syntetiske brændstoffer kan mindske CO2-fodaftrykketKredit:CC0 Public Domain Syntetiske brændstoffer, lavet ved hjælp af kulstof fanget fra luften, landbrugsaffald eller biomasse, kunne hjælpe transportsektoren med at reducere sin afhængighed af fo
Syntetiske brændstoffer kan mindske CO2-fodaftrykketKredit:CC0 Public Domain Syntetiske brændstoffer, lavet ved hjælp af kulstof fanget fra luften, landbrugsaffald eller biomasse, kunne hjælpe transportsektoren med at reducere sin afhængighed af fo -
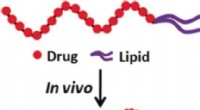 Transport af lipidkonjugeret floxuridin med naturligt serumalbumin til levering til kræftcellerKredit:Wiley Hvordan kan eliminering af terapeutiske midler fra blodbanen eller deres tidlige enzymatiske nedbrydning undgås ved systemisk levering? Kinesiske forskere har nyudviklet en metode til
Transport af lipidkonjugeret floxuridin med naturligt serumalbumin til levering til kræftcellerKredit:Wiley Hvordan kan eliminering af terapeutiske midler fra blodbanen eller deres tidlige enzymatiske nedbrydning undgås ved systemisk levering? Kinesiske forskere har nyudviklet en metode til -
 Lille molekyle transporterer jern i mus, menneskelige celler til behandling af visse former for anæ…Kredit:Pixabay/CC0 Public Domain Et naturligt lille molekyle afledt af et cyprestræ kan transportere jern i levende mus og menneskeceller, der mangler det protein, der normalt gør arbejdet, hvilket
Lille molekyle transporterer jern i mus, menneskelige celler til behandling af visse former for anæ…Kredit:Pixabay/CC0 Public Domain Et naturligt lille molekyle afledt af et cyprestræ kan transportere jern i levende mus og menneskeceller, der mangler det protein, der normalt gør arbejdet, hvilket -
 Muslinger inspirerer til ny teknologi, der kan hjælpe med at rense vand og rense oliespildKredit:CC0 Public Domain Muslinger er berygtede maritime blindpassagerer kendt for at beskadige bådenes skrog, men de samme klæbeegenskaber har udbredte tekniske anvendelser, Det skriver videnskab
Muslinger inspirerer til ny teknologi, der kan hjælpe med at rense vand og rense oliespildKredit:CC0 Public Domain Muslinger er berygtede maritime blindpassagerer kendt for at beskadige bådenes skrog, men de samme klæbeegenskaber har udbredte tekniske anvendelser, Det skriver videnskab


