Lille molekyle transporterer jern i mus, menneskelige celler til behandling af visse former for anæmi
Kredit:Pixabay/CC0 Public Domain
Et naturligt lille molekyle afledt af et cyprestræ kan transportere jern i levende mus og menneskeceller, der mangler det protein, der normalt gør arbejdet, hvilket letter en ophobning af jern i leveren og genopretter produktionen af hæmoglobin og røde blodlegemer, viser en ny undersøgelse.
Med udgangspunkt i et samarbejde mellem forskere ved University of Illinois Urbana Champaign, University of Michigan, Ann Arbor og University of Modena i Italien, viste undersøgelsen, at det lille molekyle hinokitiol potentielt kunne fungere som en "molekylær protese", når jern- transport af protein ferroportin mangler eller er defekt, hvilket tilbyder en potentiel behandlingsvej for ferroportins sygdom og visse former for anæmi.
"Dette er en virkelig slående demonstration i en hel dyremodel, at en ufuldkommen efterligning af et manglende protein kan genetablere fysiologien og fungere som en protese på molekylær skala," siger studieleder Dr. Martin D. Burke, professor i kemi i Illinois og medlem af Carle Illinois College of Medicine, samt en læge. "Implikationerne er egentlig ret brede med hensyn til andre sygdomme forårsaget af tab af proteinfunktion."
Ferroportin er et protein, der danner en kanal til transport af jern ind og ud af celler. Ferroportin-mangel kan skyldes en genetisk mutation eller forårsaget af betændelse eller infektion. Patienter uden proteinet har en overskydende ophobning af jern i leveren, milten og knoglemarven, især i en celletype kaldet en makrofag. Makrofager i leveren tygger gamle røde blodlegemer op og transporterer jernet i dem til genbrug til nye røde blodlegemer. Men uden ferroportin opbygges jernet inde i cellerne og kan ikke genbruges, sagde Burke.
At fjerne blod fra kroppen, som det normalt gøres for andre sygdomme forårsaget af jernophobning, er ikke en effektiv behandling, da ophobningen er lokaliseret, og jernniveauet i blodet faktisk er lavt, sagde undersøgelsens medforfatter Dr. Antonello Pietrangelo, en professor medicin i Modena. Pietrangelo var den første til at identificere genetisk ferroportin-sygdom hos patienter til forskel fra en mere veldokumenteret form for jernoverbelastning, der får jern til at ophobes i blodserum.
Burkes gruppe i Illinois detaljerede hinokitiols evne til at transportere jern gennem cellemembraner og korrigere anæmi hos zebrafisk i 2017, hvilket etablerede det som en potentiel kandidat til terapeutisk anvendelse. I den nye undersøgelse, offentliggjort i tidsskriftet PNAS , undersøgte forskere hinokitiols virkning i levende mus, der mangler genet for ferroportin, såvel som i makrofager fra patienter med ferroportins sygdom.
Michigan-professor Young-Ah Seos forskningsgruppe, som studerer genetiske lidelser i jern og mangan, gav bevis for, at hinokitiol kunne forbedre anæmi hos mus.
"Vi så, at musene, der blev behandlet med hinokitiol, reducerede jernophobning i leveren og forbedrede produktionen af hæmoglobin og røde blodlegemer," siger Seo, professor i ernæringsbiokemi og medforfatter af undersøgelsen. "Disse resultater tyder på, at hinokitiol kunne levere jern fra leveren til røde blodlegemer og dermed forbedre hæmoglobin hos mus."
Forskerne bemærkede, at selvom jernfordelingen stadig ikke var normal hos mus behandlet med hinokitiol, var hæmoglobin- og røde blodlegemer forbedret til normalområdet. Dette indikerer, at det lille molekyle, selvom det ikke er en perfekt erstatning for ferroportin, effektivt kan behandle anæmi, sagde Illinois-kandidatstuderende Stella Ekaputri, den første forfatter til undersøgelsen.
"I sunde organismer er der en tærskel for funktionalitet. Vores mål er at give en lille smule boost, så tærsklen nås," sagde Ekaputri. "Selvom vores lille molekyle ikke er perfekt, genvindes homeostase for hæmoglobin. Bare en lille smule boost er nok til at overvinde de flaskehalse, der skabes af ferroportin-manglen."
Forskerne gravede dybere for at forstå mekanismerne for, hvordan hinokitiol styrkede jerntransport og hæmoglobinproduktion hos mus. De fandt ud af, at hinokitiol bandt sig til jern i makrofagerne, hvor det havde opbygget sig og transporterede jernet ud af cellerne. Derefter afleverede hinokitiol jernet til et andet protein, transferrin, som indsatte jernet tilbage i den normale hæmoglobin-produktionscyklus, fandt forskerne.
Forskerne bekræftede, at hinokitiol fungerede på samme måde i humane celler ved at studere dets virkning i levermakrofager fra humane patienter med ferroportin-sygdom.
"Ved at bruge vores patienters makrofager var vi i stand til at vise, at hinokitiol meget effektivt kan fjerne 'frit jern' og også jernlagre fra makrofager fra patienter med forskellige mutationer," sagde Pietrangelo. "Dette, kombineret med data fra mus, der viser, at hinokitiol også er effektiv in vivo, åbner en helt ny vej til behandling af denne lidelse." + Udforsk yderligere
Forskere finder nøglemolekyle, der kan føre til nye behandlinger mod anæmi
 Varme artikler
Varme artikler
-
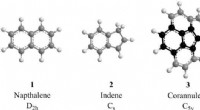 Interstellar kemi:lavtemperaturgasfasedannelse af inden i det interstellare mediumDe enkleste repræsentanter for to-ring PAHer, der bærer to seks-leddede (naphthalen, C10H8; 1) og en seks- sammen med en fem-leddet ring (indene, C9H8; 2). Mens hydrogenabstraktion-vinylacetylen-addit
Interstellar kemi:lavtemperaturgasfasedannelse af inden i det interstellare mediumDe enkleste repræsentanter for to-ring PAHer, der bærer to seks-leddede (naphthalen, C10H8; 1) og en seks- sammen med en fem-leddet ring (indene, C9H8; 2). Mens hydrogenabstraktion-vinylacetylen-addit -
 Tilberedning af melorme til en velsmagende, sund, kødlignende krydderiMelorme (Tenebrio molitor). Kredit:Pengo/Wikimedia CC BY-SA 3.0 Billelarver, såsom melorme, anses ofte for at være uhyggelige, krybende gener. Men disse insekter er spiselige og kan være et sundt a
Tilberedning af melorme til en velsmagende, sund, kødlignende krydderiMelorme (Tenebrio molitor). Kredit:Pengo/Wikimedia CC BY-SA 3.0 Billelarver, såsom melorme, anses ofte for at være uhyggelige, krybende gener. Men disse insekter er spiselige og kan være et sundt a -
 Sådan beregnes arealet af en isosceletriangelEn ensartet trekant har to lige sider. Området er det samlede rum i trekanten. Uanset om du prøver at bestemme, hvor meget mulch du skal lægge i en trekantet blomsterbed, hvor meget maling du har brug
Sådan beregnes arealet af en isosceletriangelEn ensartet trekant har to lige sider. Området er det samlede rum i trekanten. Uanset om du prøver at bestemme, hvor meget mulch du skal lægge i en trekantet blomsterbed, hvor meget maling du har brug -
 Livets oprindelse indsigt:peptider kan dannes uden aminosyrerKredit:CC0 Public Domain Peptider, en af livets grundlæggende byggesten, kan dannes ud fra de primitive forstadier til aminosyrer under forhold svarende til dem, der forventes på den oprindelige
Livets oprindelse indsigt:peptider kan dannes uden aminosyrerKredit:CC0 Public Domain Peptider, en af livets grundlæggende byggesten, kan dannes ud fra de primitive forstadier til aminosyrer under forhold svarende til dem, der forventes på den oprindelige
- Billede:Burning in Botswana
- Hvilken slags reaktion sker der med saltsyre & Alka Seltzer?
- Forskere forbedrer yderligere nøjagtigheden af retningsbestemt polarimetrisk kamera
- Multifunktionel katalysator til giftbestandige brintbrændselsceller
- Rekordhøjt arktisk ferskvand vil strømme til Labradorhavet, påvirker lokale og globale oceaner
- Attributionsvidenskab siger, at klimaændringerne er skyld i nogle ekstreme vejrbegivenheder


