Svovlelektronforstærkning:Forståelse af oktetkonfiguration
Her er hvorfor:
* Svovls elektroniske konfiguration: Svovl har 16 elektroner med den elektroniske konfiguration af [Ne] 3s² 3p⁴.
* Oktetregel: Atomer har tendens til at vinde, miste eller dele elektroner for at opnå en stabil ydre skal på 8 elektroner (oktetreglen).
* Svovls mål: Svovl har brug for yderligere to elektroner for at fylde sin 3p subshell og opnå en stabil oktetkonfiguration som ædelgassen Argon.
Derfor får svovl to elektroner til at danne en sulfidion (S²⁻).
Sidste artikelFrie radikaler:Forståelse af deres natur og virkning
Næste artikelTums:Er de sure eller alkaliske? Forståelse af antacida
 Varme artikler
Varme artikler
-
 En metode til at genvinde skjulte serienumre fra polymerprodukterGendannelse af slettede serienumre i en polymer. Kredit:American Chemical Society Polymerer er meget udbredt i industrien og anvendes i stigende grad som erstatninger for metaller ved fremstilling
En metode til at genvinde skjulte serienumre fra polymerprodukterGendannelse af slettede serienumre i en polymer. Kredit:American Chemical Society Polymerer er meget udbredt i industrien og anvendes i stigende grad som erstatninger for metaller ved fremstilling -
 Overlegen bio-blæk til 3-D-print blev banebrydendeDette 3D-printsystem ville udskrive gel stilladser, eller støttestrukturer, til dyrkning af menneskeligt væv. Ligesom traditionelle printere, der er afhængige af fire pigmenter til at dække hele farve
Overlegen bio-blæk til 3-D-print blev banebrydendeDette 3D-printsystem ville udskrive gel stilladser, eller støttestrukturer, til dyrkning af menneskeligt væv. Ligesom traditionelle printere, der er afhængige af fire pigmenter til at dække hele farve -
 Kemikere foreslår ny tilgang til syntesen af ABCD-ringsystemet af alpkinidinKredit:RUDN Universitet RUDN University kemikere, sammen med indiske kolleger fra Goa University, har syntetiseret en analog af alkaloid af alpkinidin, et stof med en signifikant cytotoksisk effek
Kemikere foreslår ny tilgang til syntesen af ABCD-ringsystemet af alpkinidinKredit:RUDN Universitet RUDN University kemikere, sammen med indiske kolleger fra Goa University, har syntetiseret en analog af alkaloid af alpkinidin, et stof med en signifikant cytotoksisk effek -
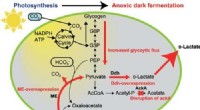 Metoden giver høj mængde af D-lactat ved hjælp af cyanobakterier, kunne revolutionere produktione…Figur 1:Vejen til omdannelse af kuldioxid til D-laktat. Synechocystis sp. PCC 6803 producerer glykogen inde i sine celler fra CO2 og lys. Det blev afsløret, at når Synechocystis sp. PCC 6803, der har
Metoden giver høj mængde af D-lactat ved hjælp af cyanobakterier, kunne revolutionere produktione…Figur 1:Vejen til omdannelse af kuldioxid til D-laktat. Synechocystis sp. PCC 6803 producerer glykogen inde i sine celler fra CO2 og lys. Det blev afsløret, at når Synechocystis sp. PCC 6803, der har
- Hvorfor et stykke jern opfører sig som magnet?
- Hvorfor ved at løfte et kilogram jern- eller fjerjernestoffer vises tungere?
- F&U-skattefradrag på statsniveau ansporer vækst af nye virksomheder:undersøgelse
- Fremtiden:Energi produceret af kæledyrs afføring?
- Forklar grundlaget for ABO -blodtyper?
- Når du blander kridt med vand og derefter fordamper, hvad har du?


