Empiriske formler i kovalente forbindelser:Kan de være ens?
Her er hvorfor:
* Empirisk formel: Den empiriske formel viser det enkleste hele talforhold mellem atomer i en forbindelse.
* Molekylformel: Molekylformlen viser det faktiske antal atomer af hvert grundstof i et molekyle.
Eksempler:
* Glucose (C6H12O6) og eddikesyre (C2H4O2): Begge har den samme empiriske formel for CH2O.
* Ethan (C2H6) og propan (C3H8): Begge har den samme empiriske formel CH3.
Årsag:
Kovalente forbindelser kan have forskellige arrangementer af atomer, hvilket fører til forskellige molekylære formler, selvom de deler det samme enkleste forhold (empirisk formel). Dette skyldes, at bindingen i kovalente forbindelser er fleksibel og kan resultere i forskellige strukturelle isomerer.
Vigtig bemærkning:
* Selvom den empiriske formel ikke fuldt ud definerer en kovalent forbindelse, kan den være nyttig til at bestemme de mulige molekylære formler.
* Bestemmelse af molekylformlen kræver yderligere oplysninger, såsom molekylmassen af forbindelsen.
 Varme artikler
Varme artikler
-
 Forbedret affaldsseparering ved hjælp af superstabil magnetisk væskeTo magnetiske væsker med en magnet i midten. Til venstre:en ustabil magnetisk væske, hvor de magnetiske partikler i væsken trækkes mod magneten. Til højre:en væske, der forbliver stabil i et magnetfel
Forbedret affaldsseparering ved hjælp af superstabil magnetisk væskeTo magnetiske væsker med en magnet i midten. Til venstre:en ustabil magnetisk væske, hvor de magnetiske partikler i væsken trækkes mod magneten. Til højre:en væske, der forbliver stabil i et magnetfel -
 Diagnosticering af kunst acne i Georgia OKeeffes malerierKig tæt på et detaljeret afsnit af Pedernal viser fremspring i mikronstørrelse fra metalsæber.Georgia OKeeffe. Pedernal, 1941. Olie på lærred, 19 x 30 1/4 tommer. Georgia OKeeffe Museum. Gave fra Geor
Diagnosticering af kunst acne i Georgia OKeeffes malerierKig tæt på et detaljeret afsnit af Pedernal viser fremspring i mikronstørrelse fra metalsæber.Georgia OKeeffe. Pedernal, 1941. Olie på lærred, 19 x 30 1/4 tommer. Georgia OKeeffe Museum. Gave fra Geor -
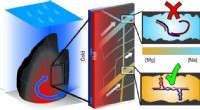 Den rigtige blanding af salte for at komme livet i gangGrafisk abstrakt. Kredit:DOI:10.1038/s41557-021-00772-5 I moderne organismer, det arvelige materiale DNA koder for instruktionerne for syntese af proteiner - de alsidige nanomaskiner, der gør det
Den rigtige blanding af salte for at komme livet i gangGrafisk abstrakt. Kredit:DOI:10.1038/s41557-021-00772-5 I moderne organismer, det arvelige materiale DNA koder for instruktionerne for syntese af proteiner - de alsidige nanomaskiner, der gør det -
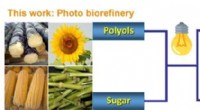 Ny fotokatalytisk metode omdanner biopolyoler og sukkerarter til methanol og syngasMetanol og syngas fungerer som platformskemikaliet, der forbinder bioraffinaderiet og petrokemisk industri. Kredit:WANG Min En forskergruppe ledet af prof. Wang Feng fra Dalian Institute of Chemic
Ny fotokatalytisk metode omdanner biopolyoler og sukkerarter til methanol og syngasMetanol og syngas fungerer som platformskemikaliet, der forbinder bioraffinaderiet og petrokemisk industri. Kredit:WANG Min En forskergruppe ledet af prof. Wang Feng fra Dalian Institute of Chemic


