Forståelse af isomerer:Molekyler med samme formel, forskellige strukturer
Isomerer er molekyler, der har samme molekylformel (samme antal af hver type atom), men forskellige strukturelle arrangementer. Disse forskellige arrangementer kan føre til væsentligt forskellige egenskaber.
Her er nogle eksempler på typer af isomerisme:
* Strukturelle isomerer: Disse har den samme molekylære formel, men adskiller sig i den måde, atomerne er forbundet på. For eksempel har butan og isobutan begge formlen C4H10, men butan har en ligekædet struktur, mens isobutan har en forgrenet struktur.
* Geometriske isomerer: Disse har den samme molekylære formel og forbindelse, men adskiller sig i det rumlige arrangement af atomer omkring en dobbeltbinding eller en ring. For eksempel har cis-2-buten og trans-2-buten begge formlen C4H8, men methylgrupperne er på samme side af dobbeltbindingen i cis-2-buten og på modsatte sider i trans-2-buten.
* Enantiomerer: Disse er stereoisomerer, der er spejlbilleder af hinanden og ikke kan overlejres. De har ofte forskellige biologiske aktiviteter. For eksempel har lægemidlet thalidomid to enantiomerer, hvoraf den ene er effektiv til behandling af morgenkvalme, mens den anden er teratogent (forårsager fødselsdefekter).
Carbons evne til at danne flere bindinger og dets tetraedriske geometri giver mulighed for en bred mangfoldighed af mulige arrangementer, hvilket fører til et stort antal isomerer. Dette er en af grundene til, at kulstof er livets rygrad og danner grundlag for så mange forskellige organiske molekyler.
 Varme artikler
Varme artikler
-
 Hvad er sjældne jordarters grundstoffer? Fire spørgsmål besvaretEn håndfuld europium. Kredit:Alchemist-hp, CC BY-SA De fleste amerikanere bruger sjældne jordarters grundstoffer hver dag – uden at vide det, eller ved noget om, hvad de laver. Det kan ændre sig,
Hvad er sjældne jordarters grundstoffer? Fire spørgsmål besvaretEn håndfuld europium. Kredit:Alchemist-hp, CC BY-SA De fleste amerikanere bruger sjældne jordarters grundstoffer hver dag – uden at vide det, eller ved noget om, hvad de laver. Det kan ændre sig, -
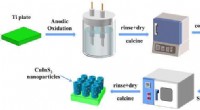 CuInS2/TiO2-fotoanodekompositter klarer sig godt i foto-induceret katodisk beskyttelseGrafisk abstrakt. Kredit:Journal of Materials Science &Technology (2022). DOI:10.1016/j.jmst.2022.02.011 Fotogenereret katodisk beskyttelsesteknologi som en værdifuld gren af fotokatalyse og foto
CuInS2/TiO2-fotoanodekompositter klarer sig godt i foto-induceret katodisk beskyttelseGrafisk abstrakt. Kredit:Journal of Materials Science &Technology (2022). DOI:10.1016/j.jmst.2022.02.011 Fotogenereret katodisk beskyttelsesteknologi som en værdifuld gren af fotokatalyse og foto -
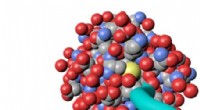 Miami kemis gennembrudsteknik muliggør design i grænsefladen mellem kemi og biologiEn syntetisk polymer (teal tube) konjugeret til et protein. Den lilla muffe på polymeren er en rapporteringsgruppe, nøglen til Konkolewicz og Pages teknik. Kredit:Miami University En teknik udvikl
Miami kemis gennembrudsteknik muliggør design i grænsefladen mellem kemi og biologiEn syntetisk polymer (teal tube) konjugeret til et protein. Den lilla muffe på polymeren er en rapporteringsgruppe, nøglen til Konkolewicz og Pages teknik. Kredit:Miami University En teknik udvikl -
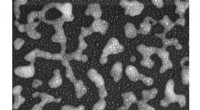 Kemisk sensing-chip opsnuser kokain inden for få minutterEt scanningselektronmikroskopbillede viser overfladen af en ny kemisk sensing-chip. Overfladen består af guld nanopartikler (små lyse prikker), der er blevet aflejret over sølv nanopartikler (lysegr
Kemisk sensing-chip opsnuser kokain inden for få minutterEt scanningselektronmikroskopbillede viser overfladen af en ny kemisk sensing-chip. Overfladen består af guld nanopartikler (små lyse prikker), der er blevet aflejret over sølv nanopartikler (lysegr


