Berylliumforbindelser:Reaktivitet og kemisk binding
* Berylliums position i det periodiske system: Beryllium er i gruppe 2 (jordalkalimetaller) og har en +2 oxidationstilstand. Dette betyder, at den let mister to elektroner for at opnå en stabil elektronkonfiguration.
* Danning af ioniske forbindelser: Beryllium danner let ioniske forbindelser med ikke-metaller, som:
* Oxygen: BeO (berylliumoxid)
* Klor: BeCl2 (berylliumchlorid)
* Svovl: BeS (berylliumsulfid)
* Danning af kovalente forbindelser: Beryllium kan også danne kovalente forbindelser med andre grundstoffer, især med halogener:
* Fluor: BeF2 (berylliumfluorid)
Vigtige bemærkninger:
* Reaktivitet: Beryllium er et relativt reaktivt metal, men det kan stabiliseres ved at danne et beskyttende oxidlag på dets overflade.
* Toksicitet: Berylliumforbindelser er giftige og kan være kræftfremkaldende. Dette skyldes berylliums lille størrelse og evne til let at trænge igennem cellemembraner.
Eksempler på almindelige berylliumforbindelser:
* Beryl: En ædelsten, der indeholder beryllium, aluminium, silicium og oxygen (Be3Al2(SiO3)6).
* Smaragd: En række af beryl med en grøn farve på grund af krom og vanadium urenheder.
* Akvamarin: En række af beryl med en blålig-grøn farve på grund af jernurenheder.
Lad mig vide, hvis du vil have flere detaljer om specifikke berylliumforbindelser!
Sidste artikelForståelse af dobbeltbindinger:definition, eksempler og egenskaber
Næste artikelIlt og mineraler:Forstå deres forhold
 Varme artikler
Varme artikler
-
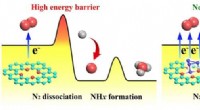 Opnåelse af højeffektiv ammoniaksyntese ved at ændre det hastighedsbestemmende trinSkematisk illustration af ændring af det hastighedsbestemmende trin i nitrogenreduktionsreaktionen ved at indføre kobolt-enkeltklynge i katalysatoren. Den cyan, rød, lilla, og grå kugler repræsenterer
Opnåelse af højeffektiv ammoniaksyntese ved at ændre det hastighedsbestemmende trinSkematisk illustration af ændring af det hastighedsbestemmende trin i nitrogenreduktionsreaktionen ved at indføre kobolt-enkeltklynge i katalysatoren. Den cyan, rød, lilla, og grå kugler repræsenterer -
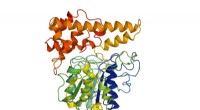 Forskere afslører bindingshemmeligheden bag proteinsuperlimDen molekylære struktur af peptidligasen ekstraheret fra den kinesiske viol (Viola yedoensis), som den laboratoriedyrkede rekombinante peptidligase var afledt af. Dette laboratoriedyrkede peptid kan h
Forskere afslører bindingshemmeligheden bag proteinsuperlimDen molekylære struktur af peptidligasen ekstraheret fra den kinesiske viol (Viola yedoensis), som den laboratoriedyrkede rekombinante peptidligase var afledt af. Dette laboratoriedyrkede peptid kan h -
 Jern-medieret kræftcelle aktivitet:En ny reguleringsmekanismeMesenkymale stamceller (til højre) er forbundet med metastatisk spredning, modstandsdygtighed over for konventionel kemoterapi og tilbagefald. Under overgangen til denne tilstand, proteinet CD44 overt
Jern-medieret kræftcelle aktivitet:En ny reguleringsmekanismeMesenkymale stamceller (til højre) er forbundet med metastatisk spredning, modstandsdygtighed over for konventionel kemoterapi og tilbagefald. Under overgangen til denne tilstand, proteinet CD44 overt -
 Praktiske videnskabsaktiviteter for at udforske frosne væskerAf Lily Mae, opdateret 30. august 2022 Når en væske bliver til et fast stof, ændres dens egenskaber på måder, der fascinerer både videnskabsmænd og studerende. Disse omhyggeligt designede eksperiment
Praktiske videnskabsaktiviteter for at udforske frosne væskerAf Lily Mae, opdateret 30. august 2022 Når en væske bliver til et fast stof, ændres dens egenskaber på måder, der fascinerer både videnskabsmænd og studerende. Disse omhyggeligt designede eksperiment
- Atomer i et mol kulstof:Forståelse af Avogadros tal
- Hvilke forskere ville være nødvendige for at bygge et atomkraftværk?
- Oversvømmelsesskove truet
- Hvad kan vi gøre for at bevare vores renere luft?
- Effekt som watt vil have på en højttaler defineres som?
- For tæt på eller for langt? Hvad frugtfluer lærer os om personligt rum


