Isotoper:Forståelse af variationer af elementer - protoner og neutroner
Isotoper er atomer af det samme grundstof med det samme antal protoner, men et andet antal neutroner.
Lad os opdele det:
* Samme element: Det betyder, at de har det samme atomnummer, som er defineret af antallet af protoner.
* Samme antal protoner: Det er som nævnt det, der bestemmer elementet.
* Forskelligt antal neutroner: Dette er den vigtigste forskel mellem isotoper. Antallet af neutroner påvirker atomets masse, men ikke dets kemiske egenskaber.
Eksempel:
Carbon-12 og Carbon-14 er isotoper af kulstof. De har begge 6 protoner (gør dem til kulstof), men kulstof-12 har 6 neutroner, mens kulstof-14 har 8 neutroner.
 Varme artikler
Varme artikler
-
 Alsidige byggesten laver strukturer med overraskende mekaniske egenskaberFire typer af diskret sammensatte mekaniske metamaterialer. Venstre til højre:Stiv, i overensstemmelse, auxetic, og chiral. (A) Som støbte ansigtsdele. (B) Single voxel, forfra. (C) En 2 × 2 × 2 terni
Alsidige byggesten laver strukturer med overraskende mekaniske egenskaberFire typer af diskret sammensatte mekaniske metamaterialer. Venstre til højre:Stiv, i overensstemmelse, auxetic, og chiral. (A) Som støbte ansigtsdele. (B) Single voxel, forfra. (C) En 2 × 2 × 2 terni -
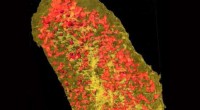 Cellemembranproteiner afbildet i 3-DUltralyse røntgenbilleder afslørede koncentrationen af erbium (gul) og zink (rød) i en enkelt E.coli-celle, der udtrykker et lanthanid-bindende mærke og inkuberet med erbium. Kredit:Brookhaven Natio
Cellemembranproteiner afbildet i 3-DUltralyse røntgenbilleder afslørede koncentrationen af erbium (gul) og zink (rød) i en enkelt E.coli-celle, der udtrykker et lanthanid-bindende mærke og inkuberet med erbium. Kredit:Brookhaven Natio -
 AI-drevet mikroskop kunne kontrollere kræftmargener på få minutterEt nyt mikroskop kaldet DeepDOF bruger kunstig intelligens til hurtigt og billigt at afbilde alle cellerne i store vævssnit (til venstre) i høj opløsning med minimal forberedelse, eliminerer den dyre
AI-drevet mikroskop kunne kontrollere kræftmargener på få minutterEt nyt mikroskop kaldet DeepDOF bruger kunstig intelligens til hurtigt og billigt at afbilde alle cellerne i store vævssnit (til venstre) i høj opløsning med minimal forberedelse, eliminerer den dyre -
 Konvertering af millimoler til milligram:en praktisk vejledningAf Sean Lancaster Opdateret 30. august 2022 Ivan-balvan/iStock/GettyImages I laboratoriemiljøer er kemiske mængder typisk udtrykt i gram. Reaktionsstøkiometri kræver dog mol - en enhed, der repræse
Konvertering af millimoler til milligram:en praktisk vejledningAf Sean Lancaster Opdateret 30. august 2022 Ivan-balvan/iStock/GettyImages I laboratoriemiljøer er kemiske mængder typisk udtrykt i gram. Reaktionsstøkiometri kræver dog mol - en enhed, der repræse
- Hvad er placeringerne i kroppen, hvor cellepopulationer gennemgår hurtig mitose?
- Hvordan havis-anomalier i Barents-Karahavet moduleres af 'varmt arktisk-koldt Eurasien'-mønster
- Hvor findes brint i hvilken formforbindelse?
- Sådan konverteres nanogrammer til Milligrams
- Interview:Airbus er klar til pilotløse jetfly – er du?
- Hvilke af følgende bølgelængdeområder kan ikke studeres med teleskoper på jorden?


