Forståelse af kaliumchlorid:hvorfor det danner ioniske bindinger
* Elektronegativitet: Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner mod sig selv i en kemisk binding.
* Kalium (K): Kalium er et metal med lav elektronegativitet. Den mister let sin ydre elektron for at opnå en stabil elektronkonfiguration.
* Klor (Cl): Klor er et ikke-metal med høj elektronegativitet. Det får let en elektron for at opnå en stabil elektronkonfiguration.
Danningen af den ioniske binding:
1. Når kalium og klor reagerer, mister kalium sin ene valenselektron og bliver til en positivt ladet ion (K+).
2. Klor får den elektron til at blive en negativt ladet ion (Cl-).
3. De modsat ladede ioner tiltrækker hinanden elektrostatisk og danner en ionbinding.
Ioniske forbindelsers egenskaber:
* Stærke elektrostatiske kræfter: Den stærke tiltrækning mellem de modsat ladede ioner giver ionforbindelser høje smelte- og kogepunkter.
* Krystallinsk struktur: Ioniske forbindelser danner en regelmæssig, tredimensionel gitterstruktur.
* Konduktivitet: Ioniske forbindelser leder elektricitet, når de er smeltet eller opløst i vand, fordi ionerne er frie til at bevæge sig.
Sammenfattende fører den betydelige forskel i elektronegativitet mellem kalium og klor til overførsel af en elektron, hvilket resulterer i dannelsen af positivt og negativt ladede ioner, der holdes sammen af stærke elektrostatiske kræfter, hvilket gør kaliumchlorid til en ionisk forbindelse.
Sidste artikelNatrium, Fluor og Neon:Forståelse af kemisk reaktivitet
Næste artikelForståelse af baser:Iondannelse og definitioner
 Varme artikler
Varme artikler
-
 Algoritmer og lasere tæmmer kemisk reaktivitetKredit:CC0 Public Domain Forskere har udviklet en algoritme til fotokemi, bringer det spirende felt et skridt nærmere målet om at bruge forskellige lysfarver som en kontakt til at aktivere en rækk
Algoritmer og lasere tæmmer kemisk reaktivitetKredit:CC0 Public Domain Forskere har udviklet en algoritme til fotokemi, bringer det spirende felt et skridt nærmere målet om at bruge forskellige lysfarver som en kontakt til at aktivere en rækk -
 Vurdering af virkningen af tabsmekanismer i solcellekandidat antimonsulfidselenidKredit:Pixabay/CC0 Public Domain Mens klimaændringer fortsætter med at præsentere sig selv som den mest presserende trussel, vores planet står over for, presser forskere på for at finde effektive o
Vurdering af virkningen af tabsmekanismer i solcellekandidat antimonsulfidselenidKredit:Pixabay/CC0 Public Domain Mens klimaændringer fortsætter med at præsentere sig selv som den mest presserende trussel, vores planet står over for, presser forskere på for at finde effektive o -
 En ny komposit til trækstyrkeStrand af menneskehår ved 200x forstørrelse. Kredit:Jan Homann/Wikipedia Materialeforskere er altid på udkig efter nye kompositter, materialer omfattende to eller flere forskellige stoffer, der ko
En ny komposit til trækstyrkeStrand af menneskehår ved 200x forstørrelse. Kredit:Jan Homann/Wikipedia Materialeforskere er altid på udkig efter nye kompositter, materialer omfattende to eller flere forskellige stoffer, der ko -
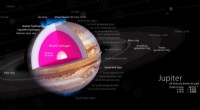 Franske forskere hævder at have skabt metallisk brintDenne udskæring illustrerer en model af det indre af Jupiter, med en stenet kerne dækket af et dybt lag flydende metallisk brint. Kredit:Kelvinsong/Wikimedia Commons Forskere har længe spekuleret
Franske forskere hævder at have skabt metallisk brintDenne udskæring illustrerer en model af det indre af Jupiter, med en stenet kerne dækket af et dybt lag flydende metallisk brint. Kredit:Kelvinsong/Wikimedia Commons Forskere har længe spekuleret
- Hvad betyder formørkelse?
- Sådan fungerer genpuljer
- Verden skal skære ned på kødforbruget for at redde klimaet:undersøgelse
- Kaster lys på den mørke side af biomassebrændende forurening
- Overfladefugtelighed har ringe effekt på atmosfærisk vandopsamling, men kantstrukturen er afgøren…
- Når politik påvirker demografien – hvordan Erdogan har bragt 10 % flere børn til Tyrkiet


