Forståelse af baser:Iondannelse og definitioner
Her er hvorfor:
* Arrhenius definition af baser: En base er et stof, der øger koncentrationen af hydroxidioner (OH-), når det opløses i vand.
* Brønsted-Lowry definition af baser: En base er et stof, der accepterer en proton (H+). Hydroxidioner er gode protonacceptorer, der danner vand (H2O).
Eksempler:
* Natriumhydroxid (NaOH): Opløses i vand for at danne natriumioner (Na+) og hydroxidioner (OH-).
* Kaliumhydroxid (KOH): Opløses i vand for at danne kaliumioner (K+) og hydroxidioner (OH-).
* Calciumhydroxid (Ca(OH)2): Opløses i vand og danner calciumioner (Ca2+) og hydroxidioner (OH-).
Mens hydroxidioner er den mest almindelige indikator for baser, kan andre ioner fungere som baser under særlige omstændigheder, især når man overvejer Brønsted-Lowry-definitionen.
Sidste artikelForståelse af kaliumchlorid:hvorfor det danner ioniske bindinger
Næste artikelThe Journey of Carbon:Hvor bliver CO2 af?
 Varme artikler
Varme artikler
-
 De tidlige stykker af livetComputerbillede, der viser fremkomsten af en rumligt organiseret informationsniche. En million tilfældige interaktioner inden for befolkningen fører til udvælgelse af visse automater, som bliver pla
De tidlige stykker af livetComputerbillede, der viser fremkomsten af en rumligt organiseret informationsniche. En million tilfældige interaktioner inden for befolkningen fører til udvælgelse af visse automater, som bliver pla -
 Ultrasmå hule legeringsnanopartikler til synergistisk hydrogenudviklingskatalyseHER-polarisationskurverne for hule PtNiCu nanopartikler, kommerciel Pt/C, hule PtCoCu nanopartikler, hule PtCu nanopartikler og Cu nanopartikler i 1,0 M KOH vandig opløsning ved en scanningshastighed
Ultrasmå hule legeringsnanopartikler til synergistisk hydrogenudviklingskatalyseHER-polarisationskurverne for hule PtNiCu nanopartikler, kommerciel Pt/C, hule PtCoCu nanopartikler, hule PtCu nanopartikler og Cu nanopartikler i 1,0 M KOH vandig opløsning ved en scanningshastighed -
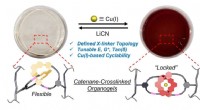 Sammenlåsende ringe låser op for nye materialeegenskaberAmatørkemikere husker måske, at kobber (Cu) normalt fremstår blåt i vand og grønt, når det er bundet af en standard ikke-aromatisk ligand. Men i tilfældet med de metalholdige catenaner, der er skabt i
Sammenlåsende ringe låser op for nye materialeegenskaberAmatørkemikere husker måske, at kobber (Cu) normalt fremstår blåt i vand og grønt, når det er bundet af en standard ikke-aromatisk ligand. Men i tilfældet med de metalholdige catenaner, der er skabt i -
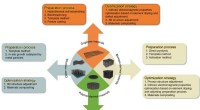 Seneste fremskridt inden for tredimensionelle porøse kulstofmaterialer til elektromagnetisk bølgea…Forskellige forberedelsesprocesser og optimeringsstrategier for 3D carbon EWAMer er opsummeret her. Kredit:Science China Press For nylig offentliggjorde professor Jiurong Liu og professor Zhihui Ze
Seneste fremskridt inden for tredimensionelle porøse kulstofmaterialer til elektromagnetisk bølgea…Forskellige forberedelsesprocesser og optimeringsstrategier for 3D carbon EWAMer er opsummeret her. Kredit:Science China Press For nylig offentliggjorde professor Jiurong Liu og professor Zhihui Ze
- Kemisk reaktion af HCl på zink?
- Facebook fremhæver tiltag for at bekæmpe 2020-desinformation
- Billede:ExoMars rover prototype
- I hvilken tilstand er de fleste elementer i?
- Hvad får hjulene til at bevæge sig på en bil?
- Hvordan valgmonitorer og udenlandsk indblanding i valgprocesser kan påvirke offentlighedens opfatte…


