Kemisk formel og dissociation:Forståelse af iondannelse
1. Identifikation af ioniske forbindelser:
* Dissociation gælder primært for ioniske forbindelser . Disse er forbindelser dannet af den elektrostatiske tiltrækning mellem positivt ladede ioner (kationer) og negativt ladede ioner (anioner).
* You can often recognize ionic compounds by looking for a metal and a non-metal in the formula.
2. Tilmeldinger i formlen:
* abonnementerne i den kemiske formel angiver antallet af hver type ion, der er til stede i forbindelsen.
* For eksempel:
* NaCl (sodium chloride):One sodium ion (Na+) and one chloride ion (Cl-) are formed when NaCl dissociates.
* CaCl2 (calciumchlorid):En calciumion (Ca2+) og to chloridioner (2Cl-) dannes, når CaCl2 dissocierer.
* Al2(SO4)3 (aluminum sulfate):Two aluminum ions (2Al3+) and three sulfate ions (3SO42-) are formed when Al2(SO4)3 dissociates.
3. Forudsigelse af dissociation:
* Opløselighedsregler help predict which ionic compounds will dissolve in water and therefore dissociate into ions.
* Ikke alle ioniske forbindelser dissocierer fuldstændigt i opløsning. Nogle kan delvist dissociere, hvilket danner en ligevægt mellem den udissocierede forbindelse og dens ioner.
Eksempel:
* Formlen for kaliumphosphat er K3PO4 .
* Dette fortæller os, at et molekyle kaliumphosphat vil dissociere i tre kaliumioner (3K+) og en fosfation (PO43-).
Opsummering:
Den kemiske formel giver værdifuld information om antallet og typer af ioner, der produceres under dissociation. Denne viden er afgørende for at forstå forskellige kemiske processer, herunder reaktioner, opløselighed og ledningsevne.
Sidste artikelHydrogenvalenselektroner:Forståelse af atomstruktur og binding
Næste artikelNitrogengas:Atom eller molekyle? Forståelse af N₂
 Varme artikler
Varme artikler
-
 En ny klasse af katalysatorer til miljøvenlige belægningerKredit:Unsplash/CC0 Public Domain Kemikere fra Konstanz har udviklet en ny klasse af katalysatorer, der gør det muligt at fremstille polyethylen-dispersioner direkte i vand. Dette åbner perspektive
En ny klasse af katalysatorer til miljøvenlige belægningerKredit:Unsplash/CC0 Public Domain Kemikere fra Konstanz har udviklet en ny klasse af katalysatorer, der gør det muligt at fremstille polyethylen-dispersioner direkte i vand. Dette åbner perspektive -
 Sådan forlænges holdbarheden og undgå madspildKredit:MIA Studio, Shutterstock Omkring en tredjedel af al mad, der produceres til konsum, går tabt eller spildes globalt hvert år, ifølge en rapport fra Food and Agricultural Organization of the
Sådan forlænges holdbarheden og undgå madspildKredit:MIA Studio, Shutterstock Omkring en tredjedel af al mad, der produceres til konsum, går tabt eller spildes globalt hvert år, ifølge en rapport fra Food and Agricultural Organization of the -
 Højre elektrolyt fordobler nye todimensionelle materialers evne til at lagre energiI denne MXene elektrode, at vælge det passende opløsningsmiddel til elektrolytten kan øge energitætheden betydeligt. Dette scanningselektronmikroskopbillede viser fine træk af en film, der kun er 5 mi
Højre elektrolyt fordobler nye todimensionelle materialers evne til at lagre energiI denne MXene elektrode, at vælge det passende opløsningsmiddel til elektrolytten kan øge energitætheden betydeligt. Dette scanningselektronmikroskopbillede viser fine træk af en film, der kun er 5 mi -
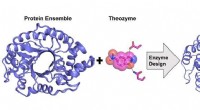 Mutanternes stigning:Ny forskning for at forbedre enzymdesignmetoderBeregningsdesign af et meget aktivt kunstigt enzym fra et proteinstrukturelt ensemble. Kredit:Rojo Rakotoharisoa En gruppe forskere ved University of Ottawa har ledt efter måder at forbedre enzymd
Mutanternes stigning:Ny forskning for at forbedre enzymdesignmetoderBeregningsdesign af et meget aktivt kunstigt enzym fra et proteinstrukturelt ensemble. Kredit:Rojo Rakotoharisoa En gruppe forskere ved University of Ottawa har ledt efter måder at forbedre enzymd
- Hvad er konsekvenserne af at bruge ikke -vedvarende energiressourcer?
- Undersøgelse afslører, hvordan havene omkring Kina reagerer på opvarmende klima
- Hvad er større økosystem eller samfund?
- Luftrensere kan gøre mere skade end gavn i lukkede rum med luftbårne vira
- Forskere udvikler teknologi til vandrensning ved elektriske udladninger
- Hvordan ændres bevægelsen af molekyler inde i en solid blokjern, som det er opvarmet?


