Valenselektroner:Hvilken gruppe har færrest?
Her er hvorfor:
* Valenselektroner er elektronerne i et atoms yderste energiniveau, og det er dem, der er involveret i kemisk binding.
* Grupper i det periodiske system er der lodrette søjler, og grundstoffer i en gruppe deler lignende kemiske egenskaber, fordi de har det samme antal valenselektroner.
* Alkalimetaller (Gruppe 1) har én valenselektron .
Andre grupper har flere valenselektroner:
* Gruppe 2 (jordalkalimetaller): To valenselektroner
* Grupper 13-18: Har henholdsvis 3-8 valenselektroner.
 Varme artikler
Varme artikler
-
 Forskere udvikler en metode til at undersøge millioner af potentielle egenproducerede lægemiddelka…Med en stor samling af fiskekroge, ETH-kemikere forsøger at fange fisken på en meget specifik måde, dvs. et molekylært mål. Kredit:ETH Zürich / Morris Köchle At lede efter nye stoffer er som at fi
Forskere udvikler en metode til at undersøge millioner af potentielle egenproducerede lægemiddelka…Med en stor samling af fiskekroge, ETH-kemikere forsøger at fange fisken på en meget specifik måde, dvs. et molekylært mål. Kredit:ETH Zürich / Morris Köchle At lede efter nye stoffer er som at fi -
 Elektricitetsdrevne undersøiske reaktioner kan have været vigtige for livets opståenForskningsgruppen har foreslået en effektiv mekanisme til at udnytte den kemiske energi, der genereres af varme hydrotermiske væsker, der strømmer ud af hydrotermiske ventilationsåbninger på Jordens t
Elektricitetsdrevne undersøiske reaktioner kan have været vigtige for livets opståenForskningsgruppen har foreslået en effektiv mekanisme til at udnytte den kemiske energi, der genereres af varme hydrotermiske væsker, der strømmer ud af hydrotermiske ventilationsåbninger på Jordens t -
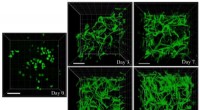 Biopolymerer til sårbehandling leverer stamceller for at forbedre helingenFigur viser det celleledende miljø af gellangummi-kollagen IPN-hydrogeler. De indkapslede fedtafledte mesenkymale stamceller (ADSCer) udviser gradvis tilbagevenden af morfologi til deres sædvanlige
Biopolymerer til sårbehandling leverer stamceller for at forbedre helingenFigur viser det celleledende miljø af gellangummi-kollagen IPN-hydrogeler. De indkapslede fedtafledte mesenkymale stamceller (ADSCer) udviser gradvis tilbagevenden af morfologi til deres sædvanlige -
 En ny metode til at udskrive spejle af variabel størrelse med en reflektionsevne på mere end 99 %Farvet spejllag printet på en folie. Inkjet-udskrivning giver mulighed for strukturering, således at store logoer også kan udskrives. Kredit:Qihao Jin, KIT Dielektriske spejle, også kaldet Bragg-sp
En ny metode til at udskrive spejle af variabel størrelse med en reflektionsevne på mere end 99 %Farvet spejllag printet på en folie. Inkjet-udskrivning giver mulighed for strukturering, således at store logoer også kan udskrives. Kredit:Qihao Jin, KIT Dielektriske spejle, også kaldet Bragg-sp
- Mirage-software automatiserer design af optiske metamaterialer
- I hvilken retning i en væske i hvile kan du bevæge dig uden at presset ændrer sig?
- Hvordan smagte romersk vin? Meget bedre end tidligere antaget, ifølge ny forskning
- Massiv lavastrøm eksploderer i havet på Hawaii (Opdatering)
- Ocean Ecosystem for Kids
- Hvad er udtrykket for materialer, der har meget lav tema energi og modstand?


