Dichromat to Chromate Conversion:Effekt af pH på chromioner
Dikromationer (Cr₂O₇²⁻) omdannes til kromationer (CrO₄²⁻).
Her er den kemiske reaktion:
Cr₂O₇²⁻ + H₂O⇌ 2CrO₄²⁻ + 2H⁺
Denne reaktion er en ligevægtsreaktion, og ligevægtspositionen skifter mod højre (begunstiger kromationer), når pH-værdien hæves.
Her er grunden:
* pH- og H⁺-koncentration: Når pH stiger, falder koncentrationen af H+-ioner.
* Le Chateliers princip: Ligevægten skifter for at lindre stress forårsaget af faldet i H⁺-koncentration. For at gøre dette forbruger reaktionen H⁺-ioner, hvilket flytter ligevægten til højre og producerer flere kromationer.
Resultat:
* Opløsningen vil ændre farve. Dikromationer er orange, mens kromationer er gule. Når pH stiger, bliver opløsningen mere gul.
Andre vigtige overvejelser:
* Ligevægtskonstant: Ligevægtskonstanten for denne reaktion er ca. 3,2 x 10⁻14, hvilket indikerer, at reaktionen stærkt favoriserer dichromationer i sure opløsninger.
* Vendbarhed: Reaktionen er reversibel. Hvis pH sænkes igen, vil reaktionen skifte tilbage til venstre, hvilket favoriserer dichromationer.
Praktiske anvendelser:
* Denne reaktion bruges i analytisk kemi til at bestemme koncentrationen af kromat- eller dichromationer.
* Farveændringen kan også bruges som en indikator i titreringer.
Sig til, hvis du har andre spørgsmål!
Sidste artikelOpløselighed:Forståelse af opløsningens grænse
Næste artikelAtommodellens udvikling:nøglevidenskabsmænd og opdagelser
 Varme artikler
Varme artikler
-
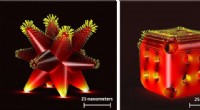 Metalkatalysatorer, der bruges til miljømæssig bæredygtighed, viste sig at nedbrydes og blive min…Nogle af de komplekse strukturelle arrangementer af katalysatorer; venstre er kendt som forgrenet struktur og højre som burstruktur. Kredit:Professor Anna Klinkova fra University of Waterloo Ny fo
Metalkatalysatorer, der bruges til miljømæssig bæredygtighed, viste sig at nedbrydes og blive min…Nogle af de komplekse strukturelle arrangementer af katalysatorer; venstre er kendt som forgrenet struktur og højre som burstruktur. Kredit:Professor Anna Klinkova fra University of Waterloo Ny fo -
 Nyt materiale slår verdensrekord for at omdanne varme til elektricitetProf. Ernst Bauer i laboratoriet. Kredit:TU Wien En ny type materiale genererer elektrisk strøm meget effektivt fra temperaturforskelle. Dette giver sensorer og små processorer mulighed for at for
Nyt materiale slår verdensrekord for at omdanne varme til elektricitetProf. Ernst Bauer i laboratoriet. Kredit:TU Wien En ny type materiale genererer elektrisk strøm meget effektivt fra temperaturforskelle. Dette giver sensorer og små processorer mulighed for at for -
 Cyanobakterier kan revolutionere plastindustrienSimpel laboratoriedyrkning af cyanobakterier i luftede rør. Kredit:Universitetet i Tübingen Cyanobakterier producerer plast naturligt som et biprodukt af fotosyntesen - og de gør det på en bæredyg
Cyanobakterier kan revolutionere plastindustrienSimpel laboratoriedyrkning af cyanobakterier i luftede rør. Kredit:Universitetet i Tübingen Cyanobakterier producerer plast naturligt som et biprodukt af fotosyntesen - og de gør det på en bæredyg -
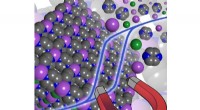 Mod næste generation af molekyle-baserede magneterBilledgengivelse af den molekylebaserede magnet og dens magnetiske egenskaber. Kredit:Rodolphe Clérac Magneter anvendes i en række teknologiske applikationer, inklusive satellitter, telefoner og k
Mod næste generation af molekyle-baserede magneterBilledgengivelse af den molekylebaserede magnet og dens magnetiske egenskaber. Kredit:Rodolphe Clérac Magneter anvendes i en række teknologiske applikationer, inklusive satellitter, telefoner og k
- NASA ser den tropiske cyklon Carlos bevæge sig forbi La Reunion Island
- Mount St.Helens 1980:Det dødeligste og mest ødelæggende vulkanudbrud i amerikansk historie
- Hvordan udøver elektriske ladninger kræfter på hinanden?
- Når en bølge bevæger sig fra mindre tæt medium til tættere, brydes det meste af energien.?
- Norges fremtidige CO2-kirkegård tager form
- Hvad er de underliggende videnskabelige principper, der bruges af Hubble -teleskop?


