Klor:Atom vs. Ion - Forståelse af kemisk binding
* Chloratom (Cl): Dette er den neutrale form af klor, der indeholder 17 protoner og 17 elektroner. Det eksisterer som et diatomisk molekyle (Cl2) i sin elementære form.
* Chlorion (Cl⁻): Dette er en negativt ladet form for klor med 17 protoner og 18 elektroner. Den får en ekstra elektron for at opnå en stabil elektronkonfiguration, hvilket gør den til en anion.
Sådan ses forskellen:
* Debitering: Et kloratom har ingen nettoladning, mens en klorion har en negativ ladning.
* Kontekst: Hvis du har at gøre med et molekyle eller en forbindelse, der indeholder klor, er klor sandsynligvis en ion. For eksempel i natriumchlorid (NaCl) eksisterer chlor som Cl⁻.
* Kemiske reaktioner: Kloratomer kan få elektroner til at danne chloridioner under kemiske reaktioner.
Opsummering: Klor kan eksistere som et neutralt atom (Cl) eller en negativt ladet ion (Cl⁻) afhængigt af dets tilstand og involvering i kemiske reaktioner.
Sidste artikelForståelse af antiaromatiske forbindelsers ustabilitet
Næste artikelMættede løsninger:definition, karakteristika og eksempler
 Varme artikler
Varme artikler
-
 Ikke så fantastisk engangsplastik for at få en miljøvenlig makeoverEn emballagefilm fremstillet af mælkeproteinet kasein er vandopløselig og biologisk nedbrydelig. Kredit:Lactips Mælkebaseret spiselig fødevareemballage og færdigretter fremstillet af træ kan være
Ikke så fantastisk engangsplastik for at få en miljøvenlig makeoverEn emballagefilm fremstillet af mælkeproteinet kasein er vandopløselig og biologisk nedbrydelig. Kredit:Lactips Mælkebaseret spiselig fødevareemballage og færdigretter fremstillet af træ kan være -
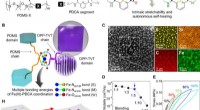 Strækbar, selvhelbredende og halvledende polymerfilm til elektronisk hud (e-skin)Design og karakterisering af belastningsfølsomme, strækbar, og selvhelbredende halvledende film. (A) Kemisk struktur af DPP halvledende polymer, PDMS, og PDCA-del introduceret i begge polymerskeletter
Strækbar, selvhelbredende og halvledende polymerfilm til elektronisk hud (e-skin)Design og karakterisering af belastningsfølsomme, strækbar, og selvhelbredende halvledende film. (A) Kemisk struktur af DPP halvledende polymer, PDMS, og PDCA-del introduceret i begge polymerskeletter -
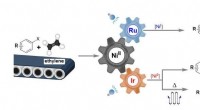 Katalytisk omdannelse af ethylenIllustration, der viser de nikkelkatalyserede reaktioner mellem kommercielt tilgængeligt arylhalogenid og ethylen. Oxidationstilstanden af nikkelkatalysatoren ændres til +1 eller 0, når den modulere
Katalytisk omdannelse af ethylenIllustration, der viser de nikkelkatalyserede reaktioner mellem kommercielt tilgængeligt arylhalogenid og ethylen. Oxidationstilstanden af nikkelkatalysatoren ændres til +1 eller 0, når den modulere -
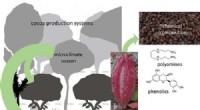 Stressede kakaotræer kan producere mere smagfuld chokoladeKredit:American Chemical Society De fleste er enige om, at chokolade smager fantastisk, men er der en måde at få det til at smage endnu bedre? Måske, ifølge forskere, der kiggede på forskellige fo
Stressede kakaotræer kan producere mere smagfuld chokoladeKredit:American Chemical Society De fleste er enige om, at chokolade smager fantastisk, men er der en måde at få det til at smage endnu bedre? Måske, ifølge forskere, der kiggede på forskellige fo
- Hvilken Rock gjorde Providence Canyon?
- Hvilken type lipider danner en levende cellemembran?
- Hvilken proces førte til dannelsen af tykke saltaflejringer, der blev fundet i grundfjorden på n…
- En ny tilgang til højeffektiv, luftstabile perovskit-solceller
- Hvorfor kinetisk energi nogensinde er større end potentiel energi?
- Hvad er proteiner, der reducerer den mængde energi, der er nødvendig for at starte en kemisk reakt…


