Bevaringslove i H₂ + Cl₂ → 2HCl-reaktionen
* Masse: Den samlede masse af reaktanterne (H2 og Cl2) er lig med den samlede masse af produktet (HCl). Dette skyldes loven om bevarelse af masse, som siger, at masse ikke kan skabes eller ødelægges i en kemisk reaktion.
* Atomer: Antallet af hydrogen- og kloratomer på reaktantsiden (2 hydrogenatomer og 2 kloratomer) er lig med antallet af hydrogen- og kloratomer på produktsiden (2 hydrogenatomer og 2 kloratomer). Dette skyldes loven om bevarelse af atomer, som siger, at atomer hverken skabes eller ødelægges i en kemisk reaktion.
* Energi: Mens reaktionen frigiver energi (den er eksoterm), forbliver systemets samlede energi konstant. Dette skyldes loven om energibevarelse, som siger, at energi ikke kan skabes eller ødelægges, kun omdannes fra en form til en anden.
Det er vigtigt at bemærke, at mens den overordnede reaktion bevarer disse mængder, kan de specifikke energiformer og atomernes arrangement ændre sig.
 Varme artikler
Varme artikler
-
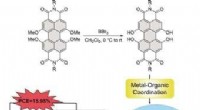 Organisk farvestof i zinkoxidmellemlag stabiliserer og øger ydeevnen af organiske solcellerKredit:Wiley Organiske solceller er lavet af billige og rigelige materialer, men deres effektivitet og stabilitet halter stadig bagefter siliciumbaserede solcellers. Et kinesisk-tysk hold af viden
Organisk farvestof i zinkoxidmellemlag stabiliserer og øger ydeevnen af organiske solcellerKredit:Wiley Organiske solceller er lavet af billige og rigelige materialer, men deres effektivitet og stabilitet halter stadig bagefter siliciumbaserede solcellers. Et kinesisk-tysk hold af viden -
 Smart lægemiddeldesign til at forhindre malariabehandlingsresistensKredit:CC0 Public Domain Resistens mod malaria kan undgås ved at studere, hvordan resistens udvikler sig under udvikling af lægemidler, ifølge et nyt blad offentliggjort i Cellekemisk biologi .
Smart lægemiddeldesign til at forhindre malariabehandlingsresistensKredit:CC0 Public Domain Resistens mod malaria kan undgås ved at studere, hvordan resistens udvikler sig under udvikling af lægemidler, ifølge et nyt blad offentliggjort i Cellekemisk biologi . -
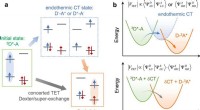 Endoterm ladningsoverførsel medierer overfladeafstandsafhængig trilling energimigrationen skematisk afbildning af de indledende og endelige tilstande og mellemliggende endoterme CT -tilstande. 3D* -A og D-3A* er de indledende og sidste tilstande, henholdsvis, der henviser til, at D −- A
Endoterm ladningsoverførsel medierer overfladeafstandsafhængig trilling energimigrationen skematisk afbildning af de indledende og endelige tilstande og mellemliggende endoterme CT -tilstande. 3D* -A og D-3A* er de indledende og sidste tilstande, henholdsvis, der henviser til, at D −- A -
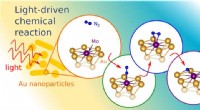 Ny proces kan reducere energibehovet fra gødning, nitrogenbaserede kemikalierNanostrukturer fremstillet af guld koncentrerer lysenergi og øger molybdænets evne til at trække de to nitrogenatomer fra hinanden i et N2 -molekyle (illustration af forskerne). Kredit:Princeton Unive
Ny proces kan reducere energibehovet fra gødning, nitrogenbaserede kemikalierNanostrukturer fremstillet af guld koncentrerer lysenergi og øger molybdænets evne til at trække de to nitrogenatomer fra hinanden i et N2 -molekyle (illustration af forskerne). Kredit:Princeton Unive
- Hvad er energitransformation i et kamera?
- Hvordan påvirker menneskelige aktiviteter plantevækst?
- Skylning af vandsystem af hjernespisende mikrobe for at tage 60 dage
- Skyrmions kan lide det varmt:Spin -strukturer kan kontrolleres, selv ved høje temperaturer
- Hvad kører på toppen af troposfæren?
- At hjælpe lærere med at 'praktisere, hvad de lærer' kan hjælpe dem med at blive undervisende i l…


