Polære opløsningsmidler:egenskaber, karakteristika og eksempler
Egenskaber af et polært opløsningsmiddel:
Polære opløsningsmidler har forskellige egenskaber på grund af deres ujævne fordeling af elektrontæthed, hvilket fører til en positiv og en negativ ende. Her er en opdeling:
1. Molekylær struktur:
* Asymmetrisk form: Polære opløsningsmidler har en ujævn fordeling af elektroner i deres molekyle, hvilket skaber et dipolmoment. Denne asymmetri resulterer ofte i bøjede eller vinklede former.
* Polære obligationer: De indeholder bindinger mellem atomer med væsentligt forskellige elektronegativiteter, hvilket fører til en adskillelse af ladninger. Eksempler omfatter oxygen-hydrogen (O-H) bindinger, nitrogen-hydrogen (N-H) bindinger og carbon-oxygen (C-O) bindinger.
2. Interaktioner:
* Hydrogenbinding: Polære opløsningsmidler kan danne stærke hydrogenbindinger med andre polære molekyler, hvilket påvirker deres egenskaber som kogepunkt og opløselighed.
* Dipol-dipol-interaktioner: De kan interagere med andre polære molekyler gennem dipol-dipol-kræfter, hvilket resulterer i stærkere intermolekylære kræfter sammenlignet med ikke-polære opløsningsmidler.
* Ion-dipol-interaktioner: Polære opløsningsmidler kan opløse ioniske forbindelser ved at tiltrække de positive og negative ioner gennem elektrostatiske interaktioner.
3. Kemiske egenskaber:
* Høj dielektrisk konstant: De har en høj dielektrisk konstant, hvilket betyder, at de kan reducere den elektrostatiske tiltrækning mellem ioner, hvilket letter opløsningen af ioniske forbindelser.
* God opløselighed: De opløser let polære molekyler som sukkerarter, alkoholer og salte på grund af de stærke interaktioner, de kan danne.
* Dårlig opløselighed af upolære stoffer: Polære opløsningsmidler kan typisk ikke opløse upolære stoffer som olier og fedtstoffer.
4. Fysiske egenskaber:
* Højt kogepunkt: På grund af stærke intermolekylære kræfter har polære opløsningsmidler en tendens til at have højere kogepunkter sammenlignet med ikke-polære opløsningsmidler.
* Høj overfladespænding: De stærke interaktioner mellem polære molekyler fører til en højere overfladespænding, hvilket gør dem mindre tilbøjelige til at fordampe.
Eksempler på polære opløsningsmidler:
* Vand (H₂O)
* Ethanol (CH₃CH₂OH)
* Acetone (CH₃COCH₃)
* Dimethylsulfoxid (DMSO)
* Eddikesyre (CH₃COOH)
Nøgleudtag:
Polære opløsningsmidler er kendetegnet ved deres evne til at danne stærke vekselvirkninger med andre polære molekyler og ioner. Deres unikke egenskaber gør dem velegnede til at opløse polære stoffer og lette kemiske reaktioner, der involverer polære arter.
 Varme artikler
Varme artikler
-
 Forskere bruger neutroner til at studere svejseinduceret stressaflastning i infrastruktur for vedvar…Colorado School of Mines kandidatstuderende forskere (til venstre) Ben Schneiderman og Tim Pickle ved hjælp af neutroner ved ORNLs High Flux Isotope Reactor til at måle restbelastning i svejsninger, d
Forskere bruger neutroner til at studere svejseinduceret stressaflastning i infrastruktur for vedvar…Colorado School of Mines kandidatstuderende forskere (til venstre) Ben Schneiderman og Tim Pickle ved hjælp af neutroner ved ORNLs High Flux Isotope Reactor til at måle restbelastning i svejsninger, d -
 Sådan beregnes luftens molære masseAf Pauline Gill Opdateret 30. august 2022 aapsky/iStock/GettyImages Molmassen af ethvert stof - fast, flydende eller gas - er massen af en mol, dvs. 6,022×10²³ enheder, af det pågældende stof. Det
Sådan beregnes luftens molære masseAf Pauline Gill Opdateret 30. august 2022 aapsky/iStock/GettyImages Molmassen af ethvert stof - fast, flydende eller gas - er massen af en mol, dvs. 6,022×10²³ enheder, af det pågældende stof. Det -
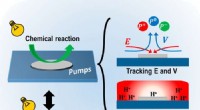 Mikropumper som en platform til forståelse af kemisk drevne mikromotorerKredit:Catalan Institute of Nanoscience and Nanotechnology Udviklingen af selvkørende mikro- og nanomaskiner, der er i stand til at efterligne den menneskelige krops og/eller det naturlige miljø
Mikropumper som en platform til forståelse af kemisk drevne mikromotorerKredit:Catalan Institute of Nanoscience and Nanotechnology Udviklingen af selvkørende mikro- og nanomaskiner, der er i stand til at efterligne den menneskelige krops og/eller det naturlige miljø -
 Lab på en chip kunne overvåge helbred, bakterier og forurenende stofferEn kunstners gengivelse af mikropartikler, der strømmer gennem en kanal og passerer gennem elektriske felter, hvor de opdages elektronisk og stregkodescannet. Kredit:Ella Marushchenko og Alexander Tok
Lab på en chip kunne overvåge helbred, bakterier og forurenende stofferEn kunstners gengivelse af mikropartikler, der strømmer gennem en kanal og passerer gennem elektriske felter, hvor de opdages elektronisk og stregkodescannet. Kredit:Ella Marushchenko og Alexander Tok
- Genbruge, reducere og genbruge videnskabsprojekter
- Undersøgelse producerer en detaljeret kemisk profil af Delhis luftforureningskilder
- Kan du tale? Apple-patent kræver iPhone-statuskontrolsystem
- Dyb læring forlænger billeddybden og fremskynder genopbygning af hologrammer
- Forklar, hvorfor den stegel-crafts-reaktion af benzen plus N-propylchlorid i nærvær Alcl3 giver fo…
- Mestring af svind:Nøjagtige beregnings- og forebyggelsestips


