Sådan beregnes luftens molære masse
Af Pauline Gill
Opdateret 30. august 2022
aapsky/iStock/GettyImages
Molmassen af ethvert stof - fast, flydende eller gas - er massen af en mol, dvs. 6,022×10²³ enheder, af det pågældende stof. Det bestemmes af summen af atommasserne af dets konstituerende atomer. For en blanding som luft er molmassen det vægtede gennemsnit af hver komponents molekylvægt, vægtet af dens volumetriske fraktion i blandingen.
Trin 1 – Identificer de vigtigste bestanddele
Luft består primært af følgende gasser (volumetriske fraktioner i forhold til 1 enhed luft):
- Nitrogen 78,09 % (0,7809)
- Oxygen 20,95 % (0,2095)
- Argon 0,933 % (0,00933)
- Kuldioxid 0,03 % (0,0003)
- Andre sporgasser:neon 0,000018, helium 0,000005, krypton 0,000001, hydrogen 0,0000005, xenon 0,09×10⁻⁶
Trin 2 – Multiplicer med molekylvægte
Fordi nitrogen (N₂) og oxygen (O₂) er diatomiske, er deres molekylvægte to gange deres atommasse:28,014 gmol-1 for N2 og 32,00 gmol-1 for O2. Beregningerne er som følger:
- Nitrogen: 28,014 × 0,7809 = 21,876
- Oxygen: 32,00 × 0,2095 = 6,704
- Argon: 39,94 × 0,00933 = 0,3726
- Kuldioxid: 44,01 × 0,0003 = 0,013
- Neon: 20,18 × 0,000018 = 3,6324 × 10⁻⁴
- Helium: 4,00 × 0,000005 = 2,0 × 10⁻⁵
- Krypton: 83,8 × 0,000001 = 8,38 × 10⁻⁵
- Brint: 2,02 × 0,0000005 = 1,01 × 10⁻⁶
- Xenon: 131,29 × 0,09 × 10⁻⁶ = 1,18 × 10⁻⁵
Trin 3 – Sum bidragene
Tilføjelse af alle de vægtede molekylvægte giver en molær luftmasse på 28,9656 gmol⁻¹. Det betyder, at et mol tør luft (6,022×10²³ molekyler) vejer 28,9656 gram under standard temperatur og tryk (STP) på 60°F og 14,696psi absolut. Ved STP optager den muldvarp 22,4L eller 0,7910ft³.
TL;DR
Oprethold ordentlig ventilation for at holde indendørs CO₂ lavt og O₂-niveauer sunde. At forstå luftens molære masse hjælper ingeniører med at designe HVAC-systemer og vurdere atmosfærisk sammensætning.
Advarsel
Kryogene gasser og væsker er ekstremt kolde og kan fryse huden på få sekunder ved kontakt. Håndter dem med passende beskyttelsesudstyr.
 Varme artikler
Varme artikler
-
 Gør trærester til smarte hydrogelerHvordan bio-hydrogeler reagerer på eksterne stimuli og i sidste ende kan nedbrydes i miljøet. Kredit:North Carolina State University NC -statens forskere gør træbiprodukter til sensoriske hydrogel
Gør trærester til smarte hydrogelerHvordan bio-hydrogeler reagerer på eksterne stimuli og i sidste ende kan nedbrydes i miljøet. Kredit:North Carolina State University NC -statens forskere gør træbiprodukter til sensoriske hydrogel -
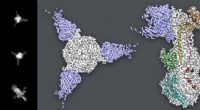 Cryo-EM-undersøgelse giver nye spor til skoldkopperinfektionBilleder ekstraheret fra cryo-EM-data (venstre og højre panel) viser varicella zoster-virusets gB-protein med tre antistoffer vedhæftet i enderne. Forskellige visninger af proteinet og antistoffer til
Cryo-EM-undersøgelse giver nye spor til skoldkopperinfektionBilleder ekstraheret fra cryo-EM-data (venstre og højre panel) viser varicella zoster-virusets gB-protein med tre antistoffer vedhæftet i enderne. Forskellige visninger af proteinet og antistoffer til -
 Neutroner sigter mod at forbedre integriteten i uens metalsvejsningerDaryush Aidun bruger HFIR-strålelinje HB-2B til at studere en forskellig svejsning af lavkulstofstål og rustfrit stål, måling af, hvor og hvordan restspændinger er fordelt i konstruktionen. Kredit:ORN
Neutroner sigter mod at forbedre integriteten i uens metalsvejsningerDaryush Aidun bruger HFIR-strålelinje HB-2B til at studere en forskellig svejsning af lavkulstofstål og rustfrit stål, måling af, hvor og hvordan restspændinger er fordelt i konstruktionen. Kredit:ORN -
 Syntetisk kanal med en stærk præference for kaliumioner tilbyder hurtig transport gennem kunstig m…Dette scanningselektronmikroskopbillede viser, at de kunstige ionkanaler selv samler sig til fibre. Kredit:American Chemical Society Kunstige ionkanaler udviklet af A*STAR-forskere kan bane vejen
Syntetisk kanal med en stærk præference for kaliumioner tilbyder hurtig transport gennem kunstig m…Dette scanningselektronmikroskopbillede viser, at de kunstige ionkanaler selv samler sig til fibre. Kredit:American Chemical Society Kunstige ionkanaler udviklet af A*STAR-forskere kan bane vejen
- Hvorfor lever mennesker?
- Væksten og faldet i Rapa Nuis-befolkningen er en lærestreg for vores fremtid
- Hvad er alt stof og energi, der findes, inklusive jordstjerner, planeter støv?
- Beregn det udførte arbejde, når 1,0 mol vand ved 273 K fordamper mod som atmosfærisk tryk atmosfæ…
- Nye detaljer bag, hvordan Shigella-patogenet leverer bakterielle proteiner ind i vores celler
- Ny teknologi er klar til at sænke omkostningerne og udvide applikationer til transparente LED -skæ…


