Sådan sammenlignes syrestyrke af forbindelser:En praktisk vejledning
Af Marissa Robert | Opdateret 30. august 2022
At bestemme, om en forbindelse er sur, basisk eller neutral, kan være så simpel som en lakmustest. Rangering af surhedsgraden af to eller flere forbindelser kræver dog lidt mere analyse. Nedenfor er en trin-for-trin tilgang, der blander kemisk intuition med praktiske værktøjer som et pH-meter.
Trin 1 – Overvej den molekylære ladning
Positivt ladede arter (protonerede molekyler eller kationer) donerer generelt protoner lettere, hvilket gør dem mere sure end neutrale molekyler. Omvendt har negativt ladede arter en tendens til at være basale.
Trin 2 – Undersøg elektronegativitet
Grundstoffet bundet til brint spiller en nøglerolle. I det periodiske system, jo længere til højre et grundstof sidder, jo stærkere trækker det elektroner mod sig selv. Et brint bundet til et meget elektronegativt atom (f.eks. fluor) vil være mere surt.
Trin 3 – Vurder atomstørrelse
Store atomer (dem nederst i det periodiske system) har en mere diffus elektronsky, som kan stabilisere den negative ladning, der bliver tilbage efter protontab. Mindre, højtliggende atomer kan holde mere fast på protonen, hvilket reducerer surhedsgraden.
Trin 4 – Evaluer molekylær geometri
Nærhed betyder noget:Jo tættere en negativt ladet gruppe (eller resonansstruktur) er på brintatomet, jo lettere kan den stabilisere den frigivne proton, hvilket øger surhedsgraden.
Trin 5 – Analyser bindingsstyrke og polarisering
Meget polariserede, skæve bindinger letter protonfrigivelse. Molekyler med flere bindinger (f.eks. alkyner) udviser ofte stærkere surhedsgrad end deres mættede modstykker på grund af øget elektrontilbagetrækning.
TL;DR (for lang; læste ikke)
Hvis der stadig er usikkerhed, bekræft din vurdering med et kalibreret pH-meter for den mest pålidelige sammenligning.
 Varme artikler
Varme artikler
-
 Kanter og hjørner øger effektiviteten af katalysatorerMed stigende ilt (rød) koncentration, der dannes en oxidsandwich på overfladen af de metalliske nanopartikler, inhibering af den ønskede reaktion af carbonmonoxid til carbondioxid. I kanterne, imidl
Kanter og hjørner øger effektiviteten af katalysatorerMed stigende ilt (rød) koncentration, der dannes en oxidsandwich på overfladen af de metalliske nanopartikler, inhibering af den ønskede reaktion af carbonmonoxid til carbondioxid. I kanterne, imidl -
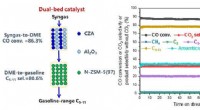 Dobbelts katalysator muliggør høj omdannelse af syngas til flydende carbonhydrider i benzininterva…Skematisk diagram for omdannelsen af syngas til flydende carbonhydrider i benzinområdet over en dobbeltbedskatalysator (CZA+Al2O3)/N-ZSM-5(97) og resultaterne af stabilitetstesten. Kredit:DICP B
Dobbelts katalysator muliggør høj omdannelse af syngas til flydende carbonhydrider i benzininterva…Skematisk diagram for omdannelsen af syngas til flydende carbonhydrider i benzinområdet over en dobbeltbedskatalysator (CZA+Al2O3)/N-ZSM-5(97) og resultaterne af stabilitetstesten. Kredit:DICP B -
 Rød, grøn, og blåt lys kan bruges til at kontrollere genekspression i manipuleret E. coliForskere fremstillede farvede billeder på kulturplader ved at bruge røde, grøn, og blåt lys til at kontrollere pigmentet produceret af bakterier med flerfarvesyn. Billedet er blevet farvekorrigeret i
Rød, grøn, og blåt lys kan bruges til at kontrollere genekspression i manipuleret E. coliForskere fremstillede farvede billeder på kulturplader ved at bruge røde, grøn, og blåt lys til at kontrollere pigmentet produceret af bakterier med flerfarvesyn. Billedet er blevet farvekorrigeret i -
 Bro over tumorvoldgrave med potente lægemiddelleveringspartiklerKredit:American Chemical Society På trods af store anstrengelser, kræft er fortsat en formidabel sygdom, med hver malign subtype, der reagerer forskelligt på terapeutika. En forhindring, der er sp
Bro over tumorvoldgrave med potente lægemiddelleveringspartiklerKredit:American Chemical Society På trods af store anstrengelser, kræft er fortsat en formidabel sygdom, med hver malign subtype, der reagerer forskelligt på terapeutika. En forhindring, der er sp
- Hvad er noget, der viser det beløb, som en kunde skylder for energi?
- Hvordan fungerer en vindvane?
- Hvad er nogle eksempler på stoffer, der er farlige for miljøet?
- Hvad er egenskaberne ved jord i tempererede regnskovsbiomer?
- Hvis du var strandet, kan du tænde en kamp på månen?
- Fald i grønt energiforbrug kan opveje emissionsfordelene fra COVID-æraen


