Surhedsniveauer for funktionelle grupper:Hvordan funktionelle grupper påvirker pH i biologiske molekyler
Af Matthew Williams
Opdateret 30. august 2022
mmoxley/iStock/GettyImages
Alt liv på Jorden er bygget af fire grundlæggende klasser af organiske molekyler - kulhydrater, lipider, proteiner og nukleinsyrer. Hver indeholder kulstof og brint, og deres egenskaber er dikteret af de funktionelle grupper knyttet til kulstofskelettet. Mens mange funktionelle grupper efterlader et molekyles surhedsgrad uændret, kan andre dramatisk ændre pH-værdien af de biologiske væsker, hvori de befinder sig. At forstå disse interaktioner er afgørende for at opretholde den fysiologiske balance.
Syrer, baser og pH-skalaen
pH-skalaen (0-14) kvantificerer koncentrationen af hydrogenioner (H⁺) i forhold til hydroxidioner (OH⁻). Ved pH 7 er antallet af H⁺ og OH⁻ ens, hvilket repræsenterer neutralitet. Stoffer, der øger H⁺-koncentrationen, sænker pH-værdien (sur, 0-6,9), mens de, der øger OH⁻ eller binder H⁺, hæver pH-værdien (basisk, 7,1-14). Jo længere en opløsnings pH afviger fra 7, jo større er den potentielle biologiske påvirkning. For eksempel har mavesyren pH 2, mens industriel lud kan overstige pH 13.
Funktionelle grupper, der ikke i væsentlig grad påvirker surhedsgraden
De fleste funktionelle grupper - såsom ketoner, simple hydroxyler, aldehyder og sulfhydryler - donerer eller accepterer generelt ikke protoner under fysiologiske forhold, så de udøver minimal indflydelse på et molekyles samlede pH. Deres elektroniske strukturer og bindingsmønstre holder dem stort set neutrale i vandige miljøer.
Carboxylgrupper (–COOH)
Carboxylgrupper er klassiske syrefunktionelle grupper. Den høje elektronegativitet af oxygenatomer stabiliserer den negative ladning, der dannes, når hydroxylhydrogenet frigives som H⁺. Denne protonfrigivelse sænker pH-værdien af den omgivende opløsning. Carboxylgrupper er til stede i fedtsyrer, fosfolipider og aminosyrer, hvilket gør dem centrale i mange biokemiske processer.
Fosfatgrupper (–PO₄³⁻)
Fosfatdele kan donere op til to protoner pr. molekyle, hvilket gør dem stærkt sure. Med fire iltatomer, der omgiver fosfor, kan molekylet stabilisere negativ ladning efter deprotonering, hvilket gør det muligt for protoner at dissociere let. Fosfater er nøglekomponenter i nukleinsyrer, ATP og mange signalmolekyler.
Aminogrupper (–NH₂)
Aminogrupper fungerer som baser:det enlige par på nitrogen kan acceptere en proton, hvilket øger den lokale pH. I aminosyrer virker carboxyl- og aminogrupperne typisk i tandem – carboxylgrupper donerer H⁺, mens aminogrupper accepterer H⁺ – hvilket ofte resulterer i en neutral nettoeffekt på pH under fysiologiske forhold.
At forstå den sure eller grundlæggende natur af funktionelle grupper hjælper kemikere og biologer med at forudsige, hvordan biomolekyler opfører sig i komplekse systemer.
 Varme artikler
Varme artikler
-
 Når man ændrer et atom, bliver molekyler bedreKredit:pexels/CC0 Udvikling og forbedring af lægemidler spiller den centrale rolle i den igangværende kamp mod sygdomme hos mennesker. Organisk syntese er det felt, der muliggør disse udviklinger,
Når man ændrer et atom, bliver molekyler bedreKredit:pexels/CC0 Udvikling og forbedring af lægemidler spiller den centrale rolle i den igangværende kamp mod sygdomme hos mennesker. Organisk syntese er det felt, der muliggør disse udviklinger, -
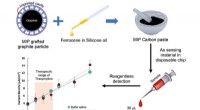 Ny grafitbaseret hurtig sensorchip til teofyllinovervågning i realtidForskere fra SIT, Japan, har designet en billig sensorchip med grafitbaseret molekylært præget polymer som elektrode. Denne chip kan bruges til at detektere og overvåge theophyllin niveauer. Kredit:Ya
Ny grafitbaseret hurtig sensorchip til teofyllinovervågning i realtidForskere fra SIT, Japan, har designet en billig sensorchip med grafitbaseret molekylært præget polymer som elektrode. Denne chip kan bruges til at detektere og overvåge theophyllin niveauer. Kredit:Ya -
 Trin-for-trin guide:Opbygning af en 3D-model af et beryllium-atomAf Michael E Carpenter Opdateret 24. marts 2022 Beryllium, eller Be, er atomnummer 4 i grundstoffernes periodiske system. Det betyder, at berylliumatomet har fire protoner og fire elektroner. Antal
Trin-for-trin guide:Opbygning af en 3D-model af et beryllium-atomAf Michael E Carpenter Opdateret 24. marts 2022 Beryllium, eller Be, er atomnummer 4 i grundstoffernes periodiske system. Det betyder, at berylliumatomet har fire protoner og fire elektroner. Antal -
 Undersøgelse opdager nyt leveringssystem, der kan hjælpe med at forhindre bakterielle infektionerKredit:CC0 Public Domain I en nylig undersøgelse i Journal of The American Chemical Society , Professor Tewodros Asefa og lektor Jeffrey Boyd syntetiserede nanostrukturerede silicapartikler, ans
Undersøgelse opdager nyt leveringssystem, der kan hjælpe med at forhindre bakterielle infektionerKredit:CC0 Public Domain I en nylig undersøgelse i Journal of The American Chemical Society , Professor Tewodros Asefa og lektor Jeffrey Boyd syntetiserede nanostrukturerede silicapartikler, ans
- Hvordan opretholdes eller opretholdes geotermisk energi?
- Hvorfor har bølger kinetisk energi?
- Forskere udvikler en reflekterende displayteknik baseret på elektro-mikrofluidisk samling af partik…
- Hvilken lov siger, at energi ikke kan oprettes eller ødelægges?
- Sådan flyder du et æg i vand
- Hvad er de vigtigste typer af gærere bioreaktorer, der bruges i dyrecellekulturproblemer, man ville…


