Reaktanter vs. produkter:Forståelse af deres roller i kemiske reaktioner
Af Michael Judge Opdateret 30. august 2022
Kemiske reaktioner er komplekse processer, der involverer kaotiske kollisioner af molekyler, hvor bindinger mellem atomer brydes og omdannes på nye måder. På trods af denne kompleksitet kan de fleste reaktioner forstås og skrives ud i grundlæggende trin, der viser en velordnet proces. Efter konvention placerer videnskabsmænd de kemikalier, der er involveret i en reaktion, i to grundlæggende kategorier:reaktanter og produkter. Dette hjælper med at forklare, hvad der sker under en reaktion, selvom virkeligheden nogle gange kan være mere kompliceret.
Kemiske reaktioner
Kemiske reaktioner
En kemisk reaktion handler for det meste om elektroner, de meget små, negativt ladede partikler, der kredser om ydersiden af alle atomer. Det er fordi elektroner danner de bindinger, der holder forskellige atomer sammen til molekyler. Elektroner hopper også fra nogle atomer til andre atomer for at danne ladede partikler kendt som ioner, der klæber sig til hinanden for at danne andre typer molekyler. I en kemisk reaktion er ændringerne mellem reaktanter og produkter, hvordan deres elektroner er blevet omarrangeret for at danne nye forbindelser mellem atomer.
Reaktanter
Reaktanter
Reaktanterne, som navnet antyder, er de kemiske elementer eller forbindelser, der reagerer sammen, og er vist på venstre side af reaktionsligningen. De ændres normalt eller nedbrydes under reaktionen og bliver derfor brugt op, efterhånden som reaktionen skrider frem. Selvom det lyder indlysende, er reaktanter ofte reaktive kemikalier, hvilket betyder, at de er lavet af arrangementer af atomer, der let går i stykker for at danne nye forbindelser. I reaktionen mellem zink (Zn) og svovlsyre (H2SO4) er disse to kemikalier reaktanterne og optræder i reaktionsligningen som Zn + H2SO4 –>.
Produkter
Produkter
Produkterne af en reaktion er de kemikalier, der dannes ved nedbrydning og omlejring af reaktanterne. De er vist i højre side af reaktionsligningen. De er generelt mere stabile molekyler end reaktanterne. I tilfælde af reaktionen mellem Zn og H2SO4 er produkterne zinksulfat og hydrogengas. Hele reaktionsligningen er skrevet som Zn + H2SO4 –> ZnSO4 + H2.
Reaktionsligevægt
Reaktionsligevægt
I tilfælde af nogle kemiske reaktioner er skelnen mellem reaktanter og produkter ikke så tydelig. Dette skyldes, at disse reaktioner eksisterer som en ligevægt, hvilket betyder, at der er en frem-og-tilbage-vej mellem reaktanter og produkter. Resultatet er, at nogle reaktanter kombineres for at producere produkter, men disse kemikalier kan derefter reagere for at reformere reaktanterne. Når først denne type reaktion når ligevægt, eksisterer både reaktanter og produkter side om side, og de konverterer konstant mellem de to tilstande.
 Varme artikler
Varme artikler
-
 Hvordan en svamp kan ødelægge immunsystemetSvampen Aspergillus fumigatus er overalt, og er ekstremt farlig for mennesker med svækket immunsystem. Det forekommer stort set overalt på Jorden, som en mørkegrå plet på fugtige vægge eller i mikrosk
Hvordan en svamp kan ødelægge immunsystemetSvampen Aspergillus fumigatus er overalt, og er ekstremt farlig for mennesker med svækket immunsystem. Det forekommer stort set overalt på Jorden, som en mørkegrå plet på fugtige vægge eller i mikrosk -
 Kemikere opdager en nøgle til grønnere fødevareproduktionSkinnende blåt lys på iridium gør det “ophidset, ”Giver den energi til at støde ind i antracenmolekylet og overføre et hydrogenatom, danner et svagt bånd. Iridiumkatalysatoren aktiverer derefter hydro
Kemikere opdager en nøgle til grønnere fødevareproduktionSkinnende blåt lys på iridium gør det “ophidset, ”Giver den energi til at støde ind i antracenmolekylet og overføre et hydrogenatom, danner et svagt bånd. Iridiumkatalysatoren aktiverer derefter hydro -
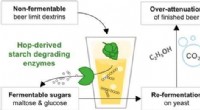 Humlet øl uden eksploderende flasker og for meget alkoholKredit:American Chemical Society Den glemte kunst at tør-hoppe øl for at forbedre smagen er tilbage på mode. Men denne praksis har undertiden uønskede bivirkninger, såsom et uventet højt alkoholin
Humlet øl uden eksploderende flasker og for meget alkoholKredit:American Chemical Society Den glemte kunst at tør-hoppe øl for at forbedre smagen er tilbage på mode. Men denne praksis har undertiden uønskede bivirkninger, såsom et uventet højt alkoholin -
 Blæksprutteskind inspirerer til skabelsen af næste generations rumtæppeAlon Gorodetsky, UCI lektor i kemisk og biomolekylær teknik, og Erica Leung, en UCI kandidatstuderende i den afdeling, har opfundet et nyt materiale, der kan fange eller frigive varme efter ønske. Kre
Blæksprutteskind inspirerer til skabelsen af næste generations rumtæppeAlon Gorodetsky, UCI lektor i kemisk og biomolekylær teknik, og Erica Leung, en UCI kandidatstuderende i den afdeling, har opfundet et nyt materiale, der kan fange eller frigive varme efter ønske. Kre
- Tyskland vil have 1 million elbiler i 2022
- Forskere finder, at seismisk billeddannelse er blind for vand
- DNA-undersøgelse viser neolitiske europæere blandet med anatolske migranter
- Kraften til attraktion, der binder modsat ladede ioner sammen?
- Hvad er forholdet mellem bindingsstyrke og mineralhårdhed?
- Hvorfor er varme den mest almindelige form for spildt energi?


