Forståelse af basedissociationskonstant (Kb) &ligevægt
Reaktionen:
```
B + H2O ⇌ BH+ + OH⁻
```
Basisdissociationskonstant (Kb):
Kb er ligevægtskonstanten for reaktionen af en svag base (B) med vand. Den måler i hvilken grad basen dissocierer i vand for at danne dens konjugerede syre (BH⁺) og hydroxidioner (OH⁻).
Formel for Kb:
```
Kb =[BH⁺] [OH⁻] / [B]
```
Hvor:
* [BH⁺] er ligevægtskoncentrationen af konjugatsyren.
* [OH⁻] er ligevægtskoncentrationen af hydroxidioner.
* [B] er ligevægtskoncentrationen af den svage base.
Forståelse af Kb:
* En større Kb-værdi indikerer en stærkere base. Dette betyder, at basen dissocierer lettere i vand, hvilket giver en højere koncentration af OH⁻-ioner.
* En mindre Kb-værdi indikerer en svagere base. Dette betyder, at basen dissocieres mindre let, hvilket resulterer i en lavere koncentration af OH⁻-ioner.
Eksempel:
Hvis du har en opløsning af en svag base med en Kb på 1,0 x 10⁻⁵, betyder det, at basen er relativt svag. Kun en lille brøkdel af basemolekylerne vil dissociere i vand for at danne de konjugerede syre- og hydroxidioner.
 Varme artikler
Varme artikler
-
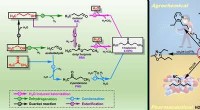 Forskere fremmer biomassetransformationsprocessen(A) Dette er en foreslået reaktionsvej, der fører til 4-HPO. (B) Dette er 4-HPO-udnyttelse. Kredit:DICP Biomasse kan tjene som en vedvarende kilde til både energi og kulstof. Acetone, n-butanol, o
Forskere fremmer biomassetransformationsprocessen(A) Dette er en foreslået reaktionsvej, der fører til 4-HPO. (B) Dette er 4-HPO-udnyttelse. Kredit:DICP Biomasse kan tjene som en vedvarende kilde til både energi og kulstof. Acetone, n-butanol, o -
 Forskere vurderer potentialet for perovskite solceller til rumapplikationerKredit:Skolkovo Institute of Science and Technology Forskere fra Skoltech, IPCP RAS, MSU og UFU har overvejet anvendelsen af nye solceller i rumfartøjer og satellitter og undersøgt strålingsstab
Forskere vurderer potentialet for perovskite solceller til rumapplikationerKredit:Skolkovo Institute of Science and Technology Forskere fra Skoltech, IPCP RAS, MSU og UFU har overvejet anvendelsen af nye solceller i rumfartøjer og satellitter og undersøgt strålingsstab -
 Ion billard cue ny materialesyntesemetodeEn skematisk illustration af den nyudviklede Proton-Driven Ion Introduction (PDII) metode. Protoner genereret ved elektrisk adskillelse af brint skydes ind i forsyningskilden for de ønskede ioner. Ion
Ion billard cue ny materialesyntesemetodeEn skematisk illustration af den nyudviklede Proton-Driven Ion Introduction (PDII) metode. Protoner genereret ved elektrisk adskillelse af brint skydes ind i forsyningskilden for de ønskede ioner. Ion -
 Cerium sidelinjen sølv for at gøre lægemiddel precursorEn mild proces opdaget af Rice University kemikere kunne erstatte vanskelige, sølvbaseret katalyse for at skabe værdifulde fluorketoner, en forløber i design og fremstilling af lægemidler. Kredit:Rene
Cerium sidelinjen sølv for at gøre lægemiddel precursorEn mild proces opdaget af Rice University kemikere kunne erstatte vanskelige, sølvbaseret katalyse for at skabe værdifulde fluorketoner, en forløber i design og fremstilling af lægemidler. Kredit:Rene
- Når kontinental skorpe og oceanisk kolliderer, hvad sker der?
- Hvad vil der ske, hvis et æble frigives fra kredsende rumskib?
- Anmeldelse:Kulterminal ville øge den globale klimaopvarmende gas
- Besynderlige radiosignaler kommer frem fra en nærliggende stjerne
- Datadrevet modellering og estimering af lithium-ion batteriets egenskaber
- Hvor stor er en transistor på et integreret kredsløb sammenlignet med hår?


