Lewis Structure of Hydrogen Chloride (HCl):En trin-for-trin guide
1. Bestem det samlede antal valenselektroner:
* Brint (H) har 1 valenselektron.
* Klor (Cl) har 7 valenselektroner.
* Samlede valenselektroner:1 + 7 =8
2. Identificer det centrale atom:
* Klor er det centrale atom, fordi det er mere elektronegativt end brint.
3. Forbind atomerne med en enkeltbinding:
* Tegn en enkelt linje mellem brint- og kloratomerne, der repræsenterer et delt elektronpar.
4. Fordel de resterende elektroner:
* Klor har brug for 6 elektroner mere for at fuldføre sin oktet (8 elektroner). Placer tre ensomme par (6 elektroner) omkring kloratomet.
* Brint har en komplet duet (2 elektroner) med enkeltbindingen.
5. Endelig Lewis-struktur:
```
H - Cl
:
:
:
```
Nøglepunkter:
* Enkeltbindingen mellem brint og klor repræsenterer et delt elektronpar, en fra hvert atom.
* Klor har tre ensomme elektronpar omkring sig.
* Strukturen viser, at både brint og klor har en stabil oktet (eller duet for brint).
Lad mig vide, hvis du gerne vil se andre eksempler på Lewis-strukturer!
Sidste artikelForstå normalitet i syrer:Hvad repræsenterer 'N'?
Næste artikelForståelse af konjugatsyrestyrke:Faktorer og eksempler
 Varme artikler
Varme artikler
-
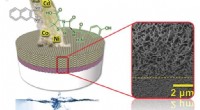 Ny, vandbaseret, genanvendelig membran filtrerer alle typer nanopartiklerEn selvsamlende membran til vandrensning. Kredit:Weizmann Institute of Science Adskillelsesteknologi er kernen i vandrensning, spildevandsrensning og genvinding af materialer, samt talrige grundlæ
Ny, vandbaseret, genanvendelig membran filtrerer alle typer nanopartiklerEn selvsamlende membran til vandrensning. Kredit:Weizmann Institute of Science Adskillelsesteknologi er kernen i vandrensning, spildevandsrensning og genvinding af materialer, samt talrige grundlæ -
 Flamme på! Hvordan AI kan tæmme en kompleks materialeteknik og transformere fremstillingJoseph Libera og Anthony Stark forbereder sig til in-situ Raman-spektroskopi. Kredit:Argonne National Laboratory Oprettelse af nanomaterialer med flammespraypyrolyse er kompleks, men forskere ved
Flamme på! Hvordan AI kan tæmme en kompleks materialeteknik og transformere fremstillingJoseph Libera og Anthony Stark forbereder sig til in-situ Raman-spektroskopi. Kredit:Argonne National Laboratory Oprettelse af nanomaterialer med flammespraypyrolyse er kompleks, men forskere ved -
 Lys i mørket:Ny opdagelse gør mikroskopisk billeddannelse mulig under mørke forholdStyring af kemiluminescens i to dimensioner. Kredit:Dr Yan Vogel, Curtin Universitet Curtin University-forskere har opdaget en ny måde at analysere mikroskopiske prøver mere nøjagtigt på ved i det
Lys i mørket:Ny opdagelse gør mikroskopisk billeddannelse mulig under mørke forholdStyring af kemiluminescens i to dimensioner. Kredit:Dr Yan Vogel, Curtin Universitet Curtin University-forskere har opdaget en ny måde at analysere mikroskopiske prøver mere nøjagtigt på ved i det -
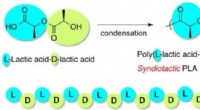 Fremgangsmåde til at syntetisere en ny polyester med alternerende arrangementFremgangsmåde til syntetisering af rene syndiotaktiske poly(mælkesyre)polyestere og billede af sfærulit deraf. Grafisk abstrakt af Polymerkemi , 2018, 9, 2446-2457. DOI:10.1039/C8PY00391B-Reproducer
Fremgangsmåde til at syntetisere en ny polyester med alternerende arrangementFremgangsmåde til syntetisering af rene syndiotaktiske poly(mælkesyre)polyestere og billede af sfærulit deraf. Grafisk abstrakt af Polymerkemi , 2018, 9, 2446-2457. DOI:10.1039/C8PY00391B-Reproducer
- Hvordan relaterer partikelhastigheden på afstanden mellem partikler?
- Forklar forholdet mellem arbejde og gravitationspotentiale energi?
- Hvorfor forekommer fusion i kernen af solen, men ikke Jupiter?
- Hvad er det ældste økosystem?
- Reduktion af omkostningerne ved strategier for at nå Paris-aftalen
- Overførsel af energi, der opstår, når en kraft påføres over afstand tomt?


