Forståelse af konjugatsyrestyrke:Faktorer og eksempler
Her er hvorfor:
* Stærkere baser har svagere konjugerede syrer. En stærk base accepterer let protoner (H+), og efterlader en relativt stabil konjugeret syre, der er mindre tilbøjelige til at donere en proton tilbage.
* Svagere baser har stærkere konjugerede syrer. En svag base er mindre tilbøjelig til at acceptere protoner, hvilket resulterer i en konjugeret syre, der er mere tilbøjelig til at donere en proton, hvilket gør den til en stærkere syre.
Eksempel:
* Stærk base: Hydroxidion (OH-)
* Svag konjugatsyre: Vand (H2O)
* Svag base: Ammoniak (NH3)
* Stærk konjugatsyre: Ammoniumion (NH4+)
For at finde den stærkeste konjugerede syre skal du vide:
1. Styrken af den tilsvarende base: Jo svagere basen er, jo stærkere er dens konjugerede syre.
2. Den specifikke kontekst: Faktorer som opløsningsmidlet og andre reagerende stoffer kan påvirke syrestyrken.
For eksempel i vandige opløsninger:
* Den stærkeste konjugerede syre ville være den konjugerede syre i den svageste base til stede. Dette kan være noget som H3O+, den konjugerede syre i vand.
Fortæl mig, hvis du har en specifik situation i tankerne, så kan jeg hjælpe dig med at bestemme den stærkeste konjugerede syre!
 Varme artikler
Varme artikler
-
 Ikke-forurenende membran til overtøjDe unge iværksættere Anna Beltzung og Mario Stucki er i startskuddet med deres membraner. Kredit:ETH Zürich / Peter Rüegg Som en del af sit kandidatprojekt, kemiingeniøren Mario Stucki udviklede e
Ikke-forurenende membran til overtøjDe unge iværksættere Anna Beltzung og Mario Stucki er i startskuddet med deres membraner. Kredit:ETH Zürich / Peter Rüegg Som en del af sit kandidatprojekt, kemiingeniøren Mario Stucki udviklede e -
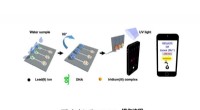 Ny enhed til hurtig og præcis detektering af blyDiagrammet viser detektionsprocessen. Kredit:HKBU Et forskerhold fra Institut for Kemi ved Hong Kong Baptist University (HKBU) har opfundet en bærbar enhed til one-stop-detektion af blykoncentrati
Ny enhed til hurtig og præcis detektering af blyDiagrammet viser detektionsprocessen. Kredit:HKBU Et forskerhold fra Institut for Kemi ved Hong Kong Baptist University (HKBU) har opfundet en bærbar enhed til one-stop-detektion af blykoncentrati -
 Ekspert:Brug af kulstof er nøglen til at dekarbonisere økonomiMatteo Pasquali fra Rice University er kemiingeniør, kemiker, materialeforsker og direktør for forskningsinitiativet Carbon Hub. Kredit:Jeff Fitlow/Rice University Rice Universitys kulstofmaterial
Ekspert:Brug af kulstof er nøglen til at dekarbonisere økonomiMatteo Pasquali fra Rice University er kemiingeniør, kemiker, materialeforsker og direktør for forskningsinitiativet Carbon Hub. Kredit:Jeff Fitlow/Rice University Rice Universitys kulstofmaterial -
 Ny undersøgelse forklarer skabelsen af geler, der frigiver pesticider og andre stoffer på en kon…Kredit:CC0 Public Domain Et hold koordineret af Santiago V. Luis og Belén Altava, fra Institut for Uorganisk og Organisk Kemi ved Universitat Jaume I, har udgivet en omfattende artikel, der omfatt
Ny undersøgelse forklarer skabelsen af geler, der frigiver pesticider og andre stoffer på en kon…Kredit:CC0 Public Domain Et hold koordineret af Santiago V. Luis og Belén Altava, fra Institut for Uorganisk og Organisk Kemi ved Universitat Jaume I, har udgivet en omfattende artikel, der omfatt
- Udforskning af effekten af ringlukning på fluorescens af supramolekylære polymerer
- Hvordan gør anderledes ljjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjjj på på…
- Hvilke energitransformationer forekommer i en hårtørrer?
- Udtynding, foreskrevne forbrændinger beskyttede skove under den massive Carlton Complex naturbrand
- Hvilke forbindelser indeholder elementet uran?
- Viskositetsvidenskabelige eksperimenter


