Rubidium-reaktivitet:Forståelse af dens høje reaktivitet
* Lav ioniseringsenergi: Den mister let sin yderste elektron og bliver til en positivt ladet ion (Rb+). Denne lette ionisering gør den meget reaktiv, især med ikke-metaller.
* Stor atomradius: Rubidiums store atomradius betyder, at dens yderste elektron er langt fra kernen og holdes mindre stramt, hvilket gør den let tabt.
* Elektropositiv natur: Rubidium er meget elektropositivt, hvilket betyder, at det har en stærk tendens til at miste elektroner og danne positive ioner.
Sådan ser dens reaktivitet ud:
* Reaktion med luft: Rubidium reagerer eksplosivt med luft, antændes spontant og danner rubidiumoxid.
* Reaktion med vand: Det reagerer voldsomt med vand, frigiver brintgas og genererer varme, der kan antænde brinten og forårsage en eksplosion.
* Reaktion med halogener: Rubidium reagerer kraftigt med halogener (som klor, brom og jod) for at danne rubidiumhalogenider.
* Reaktion med syrer: Rubidium reagerer eksplosivt med syrer og danner brintgas.
Håndtering og opbevaring:
På grund af sin ekstreme reaktivitet opbevares rubidium under inerte atmosfærer som argon eller i mineralolie for at forhindre kontakt med luft og fugt. Det kræver omhyggelig håndtering i laboratoriemiljøer for at undgå ulykker.
Applikationer:
På trods af dets reaktivitet har rubidium nicheanvendelser:
* Atomure: Rubidiums spektrale egenskaber bruges i atomure, kendt for deres høje præcision.
* Fotoceller: Rubidium bruges i nogle typer fotoceller.
* Forskning: Anvendes i forskellige forskningsområder, herunder kemi og fysik.
Opsummering: Rubidium er et meget reaktivt alkalimetal, der reagerer eksplosivt med luft, vand og mange andre stoffer. Dens reaktivitet stammer fra dens lave ioniseringsenergi, store atomradius og elektropositive natur. Selvom det er farligt at håndtere, finder det anvendelser inden for specifikke områder på grund af dets unikke egenskaber.
 Varme artikler
Varme artikler
-
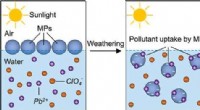 Forskere tager fat på miljøforvitring af mikroplast, optagelse af forurenende stofferGrafisk abstrakt. Kredit:ACS Environmental Au (2022). DOI:10.1021/acsenvironau.2c00036 I et nyt papir fra fakultet og studerende i LSU Chemical Engineering and Chemistry offentliggjort i ACS Enviro
Forskere tager fat på miljøforvitring af mikroplast, optagelse af forurenende stofferGrafisk abstrakt. Kredit:ACS Environmental Au (2022). DOI:10.1021/acsenvironau.2c00036 I et nyt papir fra fakultet og studerende i LSU Chemical Engineering and Chemistry offentliggjort i ACS Enviro -
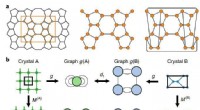 En ny matematisk tilgang til forståelse af zeolitterGraph og supercell matching. en, Repræsentation af en zeolit ved hjælp af en graf (til venstre). Enhedscellegrafen (midten) modificeres for at opfylde periodiske grænsebetingelser ved at sløjfe bind
En ny matematisk tilgang til forståelse af zeolitterGraph og supercell matching. en, Repræsentation af en zeolit ved hjælp af en graf (til venstre). Enhedscellegrafen (midten) modificeres for at opfylde periodiske grænsebetingelser ved at sløjfe bind -
 Hydrogenioners indvirkning på menneskers sundhed:Hvordan pH former vores kroppeAf John Brennan Opdateret 30. august 2022 ballero/iStock/GettyImages Når en Bronsted-syre opløses i vand, frigiver den hydrogenioner (H⁺), hvilket hæver opløsningens hydrogenionkoncentration. Kemik
Hydrogenioners indvirkning på menneskers sundhed:Hvordan pH former vores kroppeAf John Brennan Opdateret 30. august 2022 ballero/iStock/GettyImages Når en Bronsted-syre opløses i vand, frigiver den hydrogenioner (H⁺), hvilket hæver opløsningens hydrogenionkoncentration. Kemik -
 Kasseret affald kan være en skatkammer af sjældne metallerMagnetiske felter er blandt de teknikker, der udvikles til at udvinde metalpartikler fra slagger (stenet affaldsmateriale). Kredit:Slaggebunke ved Rammelsberg / Goslar af B.Nunold er licenseret under
Kasseret affald kan være en skatkammer af sjældne metallerMagnetiske felter er blandt de teknikker, der udvikles til at udvinde metalpartikler fra slagger (stenet affaldsmateriale). Kredit:Slaggebunke ved Rammelsberg / Goslar af B.Nunold er licenseret under
- Mangfoldighed eller afsavn - hvad gør et "dårligt" kvarter
- Affaldssporingssatellitter hjælper Indonesien med at tackle havaffald
- Hvis afstanden mellem stjerne en planet var 3 gange så stor, hvilken effekt ville dette have på ar…
- Hvilken ladning har 2 elektroner?
- Du ser, men finder ikke:hvorfor fraværet af beviser kan være en nyttig ting
- Sådan indsættes en absolut værdi i en Scientific Calculator


