Forbrænding af ikke-metaller:kemiske ligninger og eksempler
Ikke-metal + Oxygen → Ikke-metal Oxid
De specifikke produkter og koefficienter vil dog variere afhængigt af det specifikke ikke-metal, der er involveret. Her er nogle eksempler:
1. Forbrænding af kulstof:
C(s) + O₂(g) → CO₂(g)
2. Forbrænding af svovl:
S(s) + O₂(g) → SO2(g)
3. Forbrænding af fosfor:
4P(s) + 5O2(g) → 2P2O5(s)
4. Forbrænding af brint:
2H2(g) + O2(g) → 2H2O(g)
Vigtig bemærkning: Forbrændingen af ikke-metaller producerer ofte sure oxider. For eksempel opløses svovldioxid (SO2) i vand for at danne svovlsyrling (H2SO3).
Generelle bemærkninger:
* Eksoterm reaktion: Forbrænding er altid en eksoterm reaktion, der frigiver varme og lys.
* Oxygenkrav: Alle forbrændingsreaktioner kræver oxygen som reaktant.
* Produktdannelse: Produkterne fra ikke-metalforbrænding er normalt oxider af ikke-metallet.
* Ufuldstændig forbrænding: I nogle tilfælde kan der opstå ufuldstændig forbrænding, hvilket resulterer i dannelse af kulilte (CO) eller andre ufuldstændigt oxiderede produkter.
 Varme artikler
Varme artikler
-
 Måling af COVID-tests følsomhed med nyt materiale fra NISTNIST-materialet indeholder de to RNA-fragmenter vist her. Hvert af disse to fragmenter er omtrent 4, 000 bogstaver langt. NIST-forskere valgte at syntetisere disse særlige fragmenter, fordi de indehol
Måling af COVID-tests følsomhed med nyt materiale fra NISTNIST-materialet indeholder de to RNA-fragmenter vist her. Hvert af disse to fragmenter er omtrent 4, 000 bogstaver langt. NIST-forskere valgte at syntetisere disse særlige fragmenter, fordi de indehol -
 Kemiluminescensprober til hurtig og følsom påvisning af salmonella og listeriaKredit:CC0 Public Domain Salmonella og listeria er blandt de mest udbredte og dødeligste årsager til fødevarebårne infektioner. Deres hurtige og pålidelige registrering af fødevarer og industrielt
Kemiluminescensprober til hurtig og følsom påvisning af salmonella og listeriaKredit:CC0 Public Domain Salmonella og listeria er blandt de mest udbredte og dødeligste årsager til fødevarebårne infektioner. Deres hurtige og pålidelige registrering af fødevarer og industrielt -
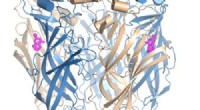 Nye molekylære designs frigør det terapeutiske potentiale af nikotinreceptorerModificerede cytisinmolekyler (fuchsia) bundet til hjernens vigtigste nikotinreceptor. Kredit:Dr. Sofia Oliveira, University of Bristol Syv millioner mennesker dør hvert år af rygerelaterede sygdo
Nye molekylære designs frigør det terapeutiske potentiale af nikotinreceptorerModificerede cytisinmolekyler (fuchsia) bundet til hjernens vigtigste nikotinreceptor. Kredit:Dr. Sofia Oliveira, University of Bristol Syv millioner mennesker dør hvert år af rygerelaterede sygdo -
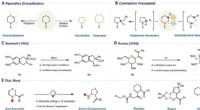 En reaktion, der fjerner svovl, nitrogen- eller oxygenatomer fra seksleddede ringe kun ved brug af b…Tilgange til piperidin-diversificering. (A) Perifer funktionalisering og skeletombygning. (B) Udvalgte eksempler på ringkontraktioner på piperidinstrukturer. (C) Grundlæggende rapport om Seebach og ko
En reaktion, der fjerner svovl, nitrogen- eller oxygenatomer fra seksleddede ringe kun ved brug af b…Tilgange til piperidin-diversificering. (A) Perifer funktionalisering og skeletombygning. (B) Udvalgte eksempler på ringkontraktioner på piperidinstrukturer. (C) Grundlæggende rapport om Seebach og ko
- Enkeltpixel-billeddannelse aktiveret af fiberlaser-arrays forventes at opnå fjerndetektering
- Hurtig kemisk forvitring kan være forårsaget af?
- Mars revisited:NASA-rumfartøjer dage væk fra risikabel landing
- Hvilke komponenter i et kredsløb forsøger at. Den elektricitet, der flyder gennem dem?
- Fordelen ved 2D metal-organiske ramme-nanoark i sanseapplikationer
- Hvad er formelnavnet på Ni2CO3?


