Beregn formelmassen af ammoniumcarbonat (NH₄)₂CO3
1. Identificer grundstofferne og deres atommasse:
* Nitrogen (N): 14,01 g/mol
* Brint (H): 1,01 g/mol
* Kulstof (C): 12,01 g/mol
* Oxygen (O): 16,00 g/mol
2. Tæl antallet af atomer i hvert grundstof:
* Nitrogen (N): 2
* Brint (H): 8 (4 x 2)
* Kulstof (C): 1
* Oxygen (O): 3
3. Gang antallet af atomer i hvert grundstof med dets atommasse:
* Nitrogen: 2 atomer * 14,01 g/mol/atom =28,02 g/mol
* Brint: 8 atomer * 1,01 g/mol/atom =8,08 g/mol
* Kulstof: 1 atom * 12,01 g/mol/atom =12,01 g/mol
* Oxygen: 3 atomer * 16,00 g/mol/atom =48,00 g/mol
4. Tilføj masserne af alle elementerne sammen:
28,02 g/mol + 8,08 g/mol + 12,01 g/mol + 48,00 g/mol =96,11 g/mol
Derfor er formelmassen af ammoniumcarbonat ((NH₄)₂CO₃) 96,11 g/mol.
 Varme artikler
Varme artikler
-
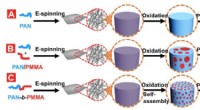 Forskere skaber de første kulfibre med ensartet porøs strukturKonventionel (A, B) og nye (C) metoder til syntetisering af kulfibre fra forskellige polymerprækursorer. (A) Pure PAN er elektrospundet ind i en fibermåtte, oxideret ved 280 °C i luft for at tværbinde
Forskere skaber de første kulfibre med ensartet porøs strukturKonventionel (A, B) og nye (C) metoder til syntetisering af kulfibre fra forskellige polymerprækursorer. (A) Pure PAN er elektrospundet ind i en fibermåtte, oxideret ved 280 °C i luft for at tværbinde -
 Broget besætning:Rust og lys er et muligt svar på gåden med produktion af brintbrændstofUdarbejdelse af en ny og effektiv måde at producere brint fra organisk affald. Kredit:Tokyo University of Science I dagens fortælling om klimaændringer, forurening, og reducerede ressourcer, ét br
Broget besætning:Rust og lys er et muligt svar på gåden med produktion af brintbrændstofUdarbejdelse af en ny og effektiv måde at producere brint fra organisk affald. Kredit:Tokyo University of Science I dagens fortælling om klimaændringer, forurening, og reducerede ressourcer, ét br -
 Forskning baner vej for næste generation af screeningsenheder for krystallinsk materialeEn illustration af den kontinuerlige mikrofluidiske enhed til hurtig screening af krystaller af aktive farmaceutiske ingredienser. Når krystaller vokser, automatiseret dataindsamling og parallel behan
Forskning baner vej for næste generation af screeningsenheder for krystallinsk materialeEn illustration af den kontinuerlige mikrofluidiske enhed til hurtig screening af krystaller af aktive farmaceutiske ingredienser. Når krystaller vokser, automatiseret dataindsamling og parallel behan -
 Almindelige polyatomiske ioner i hverdagsforbindelserAf Matthew Perdue – Opdateret 24. marts 2022 En polyatomisk ion er en ladet gruppe af mindst to kovalent bundne atomer. Mens de fleste har en negativ ladning, er nogle, som ammonium, positivt ladede
Almindelige polyatomiske ioner i hverdagsforbindelserAf Matthew Perdue – Opdateret 24. marts 2022 En polyatomisk ion er en ladet gruppe af mindst to kovalent bundne atomer. Mens de fleste har en negativ ladning, er nogle, som ammonium, positivt ladede


