Almindelige polyatomiske ioner i hverdagsforbindelser
Af Matthew Perdue – Opdateret 24. marts 2022
En polyatomisk ion er en ladet gruppe af mindst to kovalent bundne atomer. Mens de fleste har en negativ ladning, er nogle, som ammonium, positivt ladede kationer. Disse ioner danner rygraden i mange velkendte uorganiske forbindelser.
Natriumhydroxid (NaOH)
NaOH består af en natriumkation (Na + ) og en hydroxidanion (OH - ). Hydroxidionen donerer med en enkelt ekstra elektron den elektron til natriumionen, hvilket skaber en neutral ionforbindelse, der er meget udbredt som en stærk base.
Calciumcarbonat (CaCO₃)
CaCO₃ er en nøglekomponent i kalksten, skaller og tandemalje. Den har en calciumkation (Ca 2+ ) bundet til en carbonatanion (CO3 2- ), hvor carbonationens to ekstra elektroner balancerer calciums to positive ladninger.
Syrer indeholdende polyatomiske ioner
Mange syrer – såsom fosforsyre (H3 PO4 ), nitrat (HNO3 ) og svovlsyre (H2 SO4 ) – er bygget op omkring polyatomiske ioner (PO4 3- , NEJ3 - , SO4 2- ). I vandig opløsning dissocierer disse syrer og frigiver H + ioner, hvis koncentration bestemmer pH.
Ammonium (NH4 + )
Ammonium er den mest almindelige positivt ladede polyatomiske ion. Dannet af et nitrogenatom bundet til fire hydrogenatomer, bærer det en +1 ladning og parrer sig let med anioner som nitrat for at danne forbindelser som ammoniumnitrat (NH4 NEJ3 ).
Forståelse af polyatomiske ioners adfærd giver indsigt i strukturen og reaktiviteten af utallige kemiske stoffer, man støder på dagligt.
 Varme artikler
Varme artikler
-
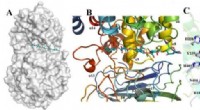 Strukturer i tang kaster lys over bæredygtighedOverfladerepræsentation og substratbindingsrille på Dp0100 Kredit:JI Shiqi Brunalger er ikke bare tang, der flyder i havet og floker svømmernes fødder - de indeholder også en hemmelighed. I sin ce
Strukturer i tang kaster lys over bæredygtighedOverfladerepræsentation og substratbindingsrille på Dp0100 Kredit:JI Shiqi Brunalger er ikke bare tang, der flyder i havet og floker svømmernes fødder - de indeholder også en hemmelighed. I sin ce -
 Sveden er en eksoterm proces, der holder os køligegorodenkoff/iStock/GettyImages Sveden er en naturlig reaktion på varme, fysisk anstrengelse eller følelsesmæssig stress. Når vores kropstemperatur stiger, udløser nervesystemet svedkirtlerne til at f
Sveden er en eksoterm proces, der holder os køligegorodenkoff/iStock/GettyImages Sveden er en naturlig reaktion på varme, fysisk anstrengelse eller følelsesmæssig stress. Når vores kropstemperatur stiger, udløser nervesystemet svedkirtlerne til at f -
 Hemmeligheden bag årstidens bedste varm chokolade? Det hele ligger i kemien!For Gregory Limburn, glæden ved varm chokolade er den hemmelige videnskab, der går ind for at skabe den. Kredit:University of Southampton Varm chokolade kan spore sine rødder til de svundne dage i
Hemmeligheden bag årstidens bedste varm chokolade? Det hele ligger i kemien!For Gregory Limburn, glæden ved varm chokolade er den hemmelige videnskab, der går ind for at skabe den. Kredit:University of Southampton Varm chokolade kan spore sine rødder til de svundne dage i -
 Undersøisk liv lover at dræbe tuberkuloseDr. Rohde og hans team arbejder på at afdække hemmelighederne bag svampe og andet undersøisk liv, der kan hjælpe med at bekæmpe tuberkulose. Kredit:University of Central Florida Et team af forsker
Undersøisk liv lover at dræbe tuberkuloseDr. Rohde og hans team arbejder på at afdække hemmelighederne bag svampe og andet undersøisk liv, der kan hjælpe med at bekæmpe tuberkulose. Kredit:University of Central Florida Et team af forsker
- Hvordan neutraliserer landmænd jord, der er sur?
- Beskriv jordens vigtigste kilder til intern og ekstern energi?
- Hvad findes de fælles konstellationer i himlen?
- Kina opsender Mars-sonden i rumkapløb med USA
- Hvorfor stiger opløseligheden af jod i vand, når koncentration af kaliumiodid øges?
- Hvilken formel opladning har kulstof?


