Hydrogens Valence forklaret:Hvorfor det er en og dets indvirkning på kemi
Af Kevin Carr – Opdateret 24. marts 2022
Billedkredit:luchschen/iStock/GettyImages
Atomer forbindes gennem kemiske bindinger ved at dele elektroner, en proces styret af hvert elements yderste elektronantal. Antallet af elektroner, der er tilgængelige for deling i den ydre skal, er det, kemikere kalder valensen.
TL;DR (for lang; læste ikke)
Hydrogen har sammen med alle grundstoffer i den første gruppe af det periodiske system en valens på én.
Valenselektroner
Valenselektroner er de elektroner, der bor i det højeste energiniveau, der kan deltage i kemisk binding. I kovalent kemi deles disse elektroner mellem atomer for at opfylde oktetreglen, som siger, at en stabil konfiguration normalt kræver otte elektroner i den ydre skal. Når et atom allerede har otte elektroner, opfører det sig som en ædelgas og forbliver inert. Atomer med færre end otte elektroner vil dele eller overføre elektroner for at fuldende deres oktet.
Brintens valens
Brint er et særligt tilfælde:dets 1s orbital kan kun rumme to elektroner. Den enkelte elektron i denne orbital er dens valenselektron, så hydrogens valensnummer er et. Den kan dele denne ensomme elektron med et andet atom for at fylde dens skal, eller den kan miste den for at danne en proton (H+) i sure opløsninger. På grund af denne alsidighed binder hydrogen til mange grundstoffer. For eksempel binder fire brintatomer sig til et kulstofatom (valens fire) for at danne metan (CH4), og tre brintatomer kombineres med ét nitrogenatom (valens fem) for at producere ammoniak (NH3).
Andre hydrogenforbindelser
Hydrogens evne til at dele eller donere sin valenselektron gør det muligt for det at danne både kovalente og ioniske bindinger. Det kan donere sin elektron til elektronegative atomer såsom fluor eller klor, hvilket skaber ioniske arter som HCl+. Brint kan også parre sig med sig selv for at producere H2-molekyler. I vandig opløsning mister brint ofte sin elektron og bliver til den hydron (H+), der bidrager til en opløsnings surhedsgrad.
Valens af andre elementer
Gruppe 1-elementer - inklusive lithium, natrium og kalium - har også en valens på én. Gruppe 2-elementer (beryllium, magnesium, calcium, strontium, barium) har en valens på to. Overgangsmetaller (gruppe 3-12) viser en række valenser fra én til syv, afhængigt af deres elektronkonfiguration og oxidationstilstand.
Gruppe 13-atomer (bor, aluminium) har en maksimal valens på tre. Gruppe 14-atomer (kulstof, silicium, germanium) kan nå en valens på fire. Gruppe 15 atomer (nitrogen, fosfor, arsen) maksimalt ud ved fem. Gruppe 16 atomer (ilt, svovl, selen) opnår op til seks. Gruppe 17 atomer (fluor, klor, brom) kan nå syv. Ædelgasser (gruppe 18) har otte valenselektroner, men fordi de allerede er stabile, anses de for at have en valens på nul.
 Varme artikler
Varme artikler
-
 Hår finder nye rødder som vækstmedium for urban farmingGrafisk abstrakt. Kredit:ACS Sustainable Chemistry &Engineering (2022). DOI:10.1021/acssuschemeng.2c01668 Klumperne af kasseret hår på salongulvet kan en dag hjælpe med at dyrke din frokostsalat, t
Hår finder nye rødder som vækstmedium for urban farmingGrafisk abstrakt. Kredit:ACS Sustainable Chemistry &Engineering (2022). DOI:10.1021/acssuschemeng.2c01668 Klumperne af kasseret hår på salongulvet kan en dag hjælpe med at dyrke din frokostsalat, t -
 Kunstig intelligens kan hjælpe forskere med at lave spray-on solcellerKredit:CC0 Public Domain Kunstig intelligens er måske lige noget, der accelererer spray-on solcelleteknologi, som kan revolutionere, hvordan forbrugerne bruger energi. Et forskerhold ved Universi
Kunstig intelligens kan hjælpe forskere med at lave spray-on solcellerKredit:CC0 Public Domain Kunstig intelligens er måske lige noget, der accelererer spray-on solcelleteknologi, som kan revolutionere, hvordan forbrugerne bruger energi. Et forskerhold ved Universi -
 Udviklet materiale, der er varmeisolerende og varmeledende på samme tidDet nyudviklede materiale leder varme godt langs lagene, samtidig med at den giver varmeisolering lodret. Kredit:MPI-P, Licens CC-BY-SA. Styrofoam eller kobber - begge materialer har meget forskel
Udviklet materiale, der er varmeisolerende og varmeledende på samme tidDet nyudviklede materiale leder varme godt langs lagene, samtidig med at den giver varmeisolering lodret. Kredit:MPI-P, Licens CC-BY-SA. Styrofoam eller kobber - begge materialer har meget forskel -
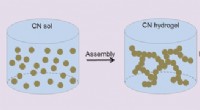 Carbonitrid aerogeler formidler den fotokatalytiske omdannelse af vandKredit:Wiley Nanokemi opfylder makrostrukturer:Kinesiske forskere rapporterer syntesen af en makroskopisk aerogel fra carbonitrid-nanomaterialer, som er en glimrende katalysator for den vandopde
Carbonitrid aerogeler formidler den fotokatalytiske omdannelse af vandKredit:Wiley Nanokemi opfylder makrostrukturer:Kinesiske forskere rapporterer syntesen af en makroskopisk aerogel fra carbonitrid-nanomaterialer, som er en glimrende katalysator for den vandopde
- En ny ungarsk metode kan hjælpe proteinforskning
- Forbrændingsdataene for en ukendt forbindelse indeholdende carbonhydrogen og ilt blev analyseret de…
- Hvad er forskellen mellem tyngdekraften til mellem elektriske ladninger?
- Har forskellige organismer stoffer inden for deres cellevægge?
- Skiftbare DNA-minimaskiner gemmer information
- Hvor mange calciumioner er der behov for for at afbalancere ladningen af en chloridion?


