Forståelse af krystalgitter i ioniske forbindelser:struktur og binding
1. Ioner: Ioniske forbindelser er opbygget af positivt ladede ioner (kationer) og negativt ladede ioner (anioner).
2. Elektrostatisk tiltrækning: De modsatte ladninger af disse ioner tiltrækker hinanden og skaber en stærk elektrostatisk kraft, der holder dem sammen.
3. Gentagende mønster: Denne tiltrækning tvinger ionerne til at arrangere sig selv i et specifikt, gentagende mønster, der danner en gitterstruktur. Dette mønster strækker sig i alle retninger og skaber et stort, indbyrdes forbundne netværk af ioner.
4. Enhedscelle: Den mindste gentagne enhed af gitteret kaldes enhedscellen. Det er som en byggesten, der, når den gentages i alle retninger, skaber hele krystalstrukturen.
5. Gitterpunkter: Placeringen af ionerne i enhedscellen kaldes gitterpunkter. Disse punkter er ikke bare tilfældige, men præcist definerede inden for krystallens tredimensionelle rum.
Hvorfor er krystalgitteret vigtigt?
* Stabilitet: Gitterstrukturen er afgørende for stabiliteten af ioniske forbindelser. Den stærke elektrostatiske tiltrækning mellem ionerne er hovedkraften, der holder sammensætningen sammen.
* Form og egenskaber: Arrangementet af ioner i gitteret bestemmer den overordnede form og fysiske egenskaber af krystallen, såsom dens smeltepunkt, hårdhed og ledningsevne.
* Reaktivitet: Gitterstrukturen kan også påvirke, hvor let en ionforbindelse reagerer med andre stoffer.
Eksempel:
Natriumchlorid (NaCl) eller bordsalt er et almindeligt eksempel på en ionisk forbindelse. Dens krystalgitter er en ansigtscentreret kubisk struktur. I denne struktur veksler natriumioner (Na+) og chloridioner (Cl-) i et tredimensionelt arrangement og danner et stabilt, gentaget mønster.
Forståelse af krystalgitre er grundlæggende for at forstå ioniske forbindelsers adfærd og egenskaber.
 Varme artikler
Varme artikler
-
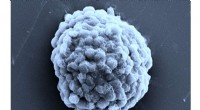 Forskning skaber brintproducerende levende dråber, bane vejen for alternativ fremtidig energikildeElektronmikroskopibillede af en tætpakket dråbe brintproducerende algeceller. Målestok, 10 mikrometer. Kredit:Prof Xin Huang, Harbin Institute of Technology Forskere har bygget små dråbebaserede m
Forskning skaber brintproducerende levende dråber, bane vejen for alternativ fremtidig energikildeElektronmikroskopibillede af en tætpakket dråbe brintproducerende algeceller. Målestok, 10 mikrometer. Kredit:Prof Xin Huang, Harbin Institute of Technology Forskere har bygget små dråbebaserede m -
 Konstrueret mikrobe kan være nøglen til at producere plastik fra planterUniversity of Wisconsin-Madison postdoc-forsker Alex Linz undersøger en tallerken strøget med N. aromaticivorans (i gult), en jordbakterie, der kunne gøre en vedvarende kilde-lignin fra planteceller
Konstrueret mikrobe kan være nøglen til at producere plastik fra planterUniversity of Wisconsin-Madison postdoc-forsker Alex Linz undersøger en tallerken strøget med N. aromaticivorans (i gult), en jordbakterie, der kunne gøre en vedvarende kilde-lignin fra planteceller -
 Smagsforskning til forbrugerbeskyttelseUdgangspunktet for undersøgelserne var en ren kirsebærjuice lavet af surkirsebær i laboratoriet. Kredit:Gisela Olias / Leibniz-LSB I 2013 den tyske Stiftung Warentest fandt skadelig benzen i drink
Smagsforskning til forbrugerbeskyttelseUdgangspunktet for undersøgelserne var en ren kirsebærjuice lavet af surkirsebær i laboratoriet. Kredit:Gisela Olias / Leibniz-LSB I 2013 den tyske Stiftung Warentest fandt skadelig benzen i drink -
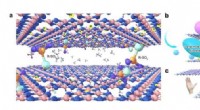 Ny membran adskiller spejlede molekyler effektivtIllustration af den chirale membran til selektiv permeation. Kredit:LIU Bos team Prof. Liu Bo og kolleger ved University of Science and Technology of China (USTC) har udviklet en chiral separation
Ny membran adskiller spejlede molekyler effektivtIllustration af den chirale membran til selektiv permeation. Kredit:LIU Bos team Prof. Liu Bo og kolleger ved University of Science and Technology of China (USTC) har udviklet en chiral separation


