Oxidationstal vs. almindelige ioner:Forstå forskellen
Oxidationsnummer:
* Definition: Repræsenterer den hypotetiske ladning et atom ville have, hvis alle dets bindinger var fuldstændig ioniske.
* Formål: At spore elektronoverførsel og bestemme, om et atom er blevet oxideret eller reduceret i en kemisk reaktion.
* Eksempler:
* I NaCl er oxidationstallet for Na +1 og Cl er -1.
* I H2O er oxidationstallet for H +1, og O er -2.
* Kan være:
* Positiv, negativ eller nul.
* Brøkdel i nogle tilfælde.
Almindelige ioner:
* Definition: Ioner, der ofte opstår i kemiske reaktioner.
* Formål: At repræsentere ladningen af et atom eller molekyle, efter at det har fået eller mistet elektroner.
* Eksempler:
* Na⁺ (natriumion)
* Cl⁻ (chloridion)
* SO₄²⁻ (sulfation)
* Er altid:
* Hele tal.
* Repræsenter den faktiske ladning af ionen i en forbindelse.
Forhold:
* Almindelige ioner har ofte samme ladning som deres oxidationstal i mange forbindelser. For eksempel er Na⁺ en almindelig ion, og dens oxidationstal i NaCl er +1.
* Oxidationsnumre kan dog tildeles atomer i molekyler, der ikke danner almindelige ioner. For eksempel har oxygen i H2O et oxidationstal på -2, selvom der ikke er nogen almindelig "oxid"-ion.
Opsummering:
Oxidationstal er et teoretisk begreb, der hjælper os med at forstå elektronoverførsel, mens almindelige ioner er faktiske ladede arter, der findes i forbindelser. De er beslægtede, men ikke identiske.
 Varme artikler
Varme artikler
-
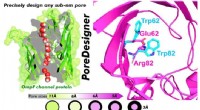 PoreDesigner forbedrer proteinkanaldesign til vandbehandling, bioseparationerFigur, der skitserer det grundlæggende i PoreDesigners arbejdsgang til ændring af porestørrelsen af et bakteriekanalprotein. Kredit:Manish Kumar / Penn State PoreDesigner, en fuldt automatiseret
PoreDesigner forbedrer proteinkanaldesign til vandbehandling, bioseparationerFigur, der skitserer det grundlæggende i PoreDesigners arbejdsgang til ændring af porestørrelsen af et bakteriekanalprotein. Kredit:Manish Kumar / Penn State PoreDesigner, en fuldt automatiseret -
 Nye fremskridt for at reducere defekter i multimaterialer ved hjælp af rettet energiaflejringIfølge undersøgelsen kan manipulation af gradientforholdet mellem komponentmaterialerne under rettet energiaflejring (en 3D-printteknik) føre til højtydende funktionelle materialer med minimale defekt
Nye fremskridt for at reducere defekter i multimaterialer ved hjælp af rettet energiaflejringIfølge undersøgelsen kan manipulation af gradientforholdet mellem komponentmaterialerne under rettet energiaflejring (en 3D-printteknik) føre til højtydende funktionelle materialer med minimale defekt -
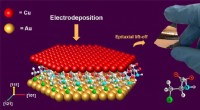 Forskere bruger aminosyrer til at dyrke højtydende kobber tynde filmKobbertynde film fremstilles ved elektroaflejring af kobber, Cu (111), på et selvsamlet organisk monolag af aminosyren L-cystein på guld, Au (111). Kredit:Bin Luo For første gang, forskere fra Mis
Forskere bruger aminosyrer til at dyrke højtydende kobber tynde filmKobbertynde film fremstilles ved elektroaflejring af kobber, Cu (111), på et selvsamlet organisk monolag af aminosyren L-cystein på guld, Au (111). Kredit:Bin Luo For første gang, forskere fra Mis -
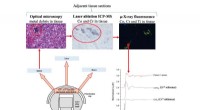 Undersøgelse af metalaflejring i organer efter ledudskiftningFigur 1:Oversigt over undersøgelsen. Kredit:Diamond Light Source Hofteprotesen anses for at være en af de mest vellykkede ortopædiske indgreb, med 75, 000 udført hvert år af NHS alene. Imidlerti
Undersøgelse af metalaflejring i organer efter ledudskiftningFigur 1:Oversigt over undersøgelsen. Kredit:Diamond Light Source Hofteprotesen anses for at være en af de mest vellykkede ortopædiske indgreb, med 75, 000 udført hvert år af NHS alene. Imidlerti
- Hvad er resultatet af ændringer i solenergi, der skaber dag og nat?
- Hvad skaber og udfører videnskabsmand for at teste deres hypoteser?
- Moderlige instinkter forklarer ikke kønsforskellen på GM-fødevarer
- Hvorfor hæmmer svampe væksten af bakterier?
- Hvilken er ikke antagelse om partikler i en gas i henhold til den kinetiske teori?
- Små mikroplastik slipper ikke længere gennem sprækkerne med en ny metode til påvisning


