Carbon Allotropes:Exploring Diamond, Graphite &Beyond
1. Diamant: En meget hård og gennemsigtig form for kulstof, hvor hvert kulstofatom er bundet til fire andre kulstofatomer i en tetraedrisk struktur. Denne stærke binding gør diamanter til det hårdeste naturligt forekommende materiale.
2. Grafit: En blød, sort og flaget form for kulstof, hvor kulstofatomer er arrangeret i lag af sekskantede ringe. Disse lag er svagt bundet, hvilket gør grafit til et godt smøremiddel og en leder af elektricitet.
3. Fullerene: En familie af kulstofmolekyler med lukkede burstrukturer, den mest berømte er Buckminsterfulleren (C60), som ligner en fodbold. Fullerener har unikke egenskaber og potentielle anvendelser inden for forskellige områder.
Andre allotropiske former for kulstof omfatter:
* Amorft kulstof: En ikke-krystallinsk form for kulstof med en uordnet struktur, som sod og trækul.
* Carbon nanorør: Cylindriske strukturer af sammenrullede grafenplader med enestående styrke og elektrisk ledningsevne.
* Graphene: Et enkelt lag af kulstofatomer arrangeret i et sekskantet gitter, kendt for dets styrke, ledningsevne og fleksibilitet.
Så mens tre allotropiske former er almindeligt nævnt, er der mange andre, hver med unikke egenskaber og applikationer.
Sidste artikelGermanium:Egenskaber, egenskaber og fysiske egenskaber
Næste artikelDiethyletherformel:Forståelse af den kemiske struktur
 Varme artikler
Varme artikler
-
 Sådan identificeres protoner, neutroner og elektroner i en isotopAtomer er sammensat af en tæt kerne, der indeholder positivt ladede protoner og elektrisk neutrale neutroner, omgivet af negativt ladede elektroner, der optager definerede orbitaler. Protoner og neutr
Sådan identificeres protoner, neutroner og elektroner i en isotopAtomer er sammensat af en tæt kerne, der indeholder positivt ladede protoner og elektrisk neutrale neutroner, omgivet af negativt ladede elektroner, der optager definerede orbitaler. Protoner og neutr -
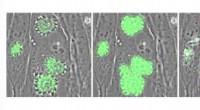 Parasitforskning varmer opIntracellulære Toxoplasma -parasitter, der udtrykker den genetisk kodede calciumindikator GCaMP. Parasitter blev behandlet med A23187, en forbindelse, der forårsager tilstrømning af calcium og stimule
Parasitforskning varmer opIntracellulære Toxoplasma -parasitter, der udtrykker den genetisk kodede calciumindikator GCaMP. Parasitter blev behandlet med A23187, en forbindelse, der forårsager tilstrømning af calcium og stimule -
 Hår finder nye rødder som vækstmedium for urban farmingGrafisk abstrakt. Kredit:ACS Sustainable Chemistry &Engineering (2022). DOI:10.1021/acssuschemeng.2c01668 Klumperne af kasseret hår på salongulvet kan en dag hjælpe med at dyrke din frokostsalat, t
Hår finder nye rødder som vækstmedium for urban farmingGrafisk abstrakt. Kredit:ACS Sustainable Chemistry &Engineering (2022). DOI:10.1021/acssuschemeng.2c01668 Klumperne af kasseret hår på salongulvet kan en dag hjælpe med at dyrke din frokostsalat, t -
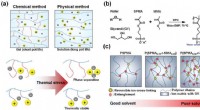 Et termometer, der kan strækkes og deformeres af vandVirkningerne af ionisk sidekæde. a) Skema, der angiver forskel med hensyn til brugstid og termisk stabilitet i henhold til kemiske og fysiske metoder. b) Skema for P(SPMA-r-MMA)er og vandopløselighed.
Et termometer, der kan strækkes og deformeres af vandVirkningerne af ionisk sidekæde. a) Skema, der angiver forskel med hensyn til brugstid og termisk stabilitet i henhold til kemiske og fysiske metoder. b) Skema for P(SPMA-r-MMA)er og vandopløselighed.


