Elementer svarende til klor:egenskaber og reaktivitet
1. Fluor (F) :Som det letteste halogen er fluor det mest reaktive ikke-metal. Det deler mange egenskaber med klor, såsom dets stærke oxidationsevne, tendens til at danne diatomiske molekyler (F2) og evnen til at danne ioniske forbindelser med metaller.
2. Brom (Br) :Lokaliseret under klor i det periodiske system, er brom en rødbrun væske ved stuetemperatur. Det har lignende kemiske egenskaber som klor, danner diatomiske molekyler (Br2) og udviser reaktivitet med metaller og andre grundstoffer.
3. Jod (I) :Jod er et fast stof ved stuetemperatur med et mørkegrå, næsten sort udseende. Det har lignende kemiske egenskaber som klor, herunder dets evne til at danne diatomiske molekyler (I2) og dets reaktivitet med metaller. Jod er dog mindre reaktivt end klor.
Nøgleligheder:
* Elektronkonfiguration: Alle halogener har 7 elektroner i deres yderste skal, hvilket giver dem lignende kemiske reaktiviteter.
* Oxidationskraft: Halogener er stærke oxidationsmidler, hvilket betyder, at de let får elektroner.
* Danning af diatomiske molekyler: Alle halogener eksisterer som diatomiske molekyler i deres elementære tilstand (F2, Cl2, Br2, I2).
* Danning af ioniske forbindelser: Halogener danner let ioniske forbindelser med metaller ved at acceptere elektroner for at opnå en stabil oktet.
Vigtig bemærkning: Mens disse elementer deler mange ligheder, kan deres egenskaber variere i intensitet på grund af forskelle i elektronegativitet, atomstørrelse og andre faktorer.
Sidste artikelKlorreaktivitet:nøgleelementer og forbindelser
Næste artikelFluors periodiske tabel Naboer:Lignende elementer og egenskaber
 Varme artikler
Varme artikler
-
 Ladningsoverførsel inden for overgangsmetalfarvestoffer analyseretEn røntgenimpuls sonderer delokaliseringen af jern-3d-elektroner på tilstødende ligander. Kredit:M. Künsting/HZB Overgangsmetalkomplekser i farvestofbaserede solceller er ansvarlige for at omdan
Ladningsoverførsel inden for overgangsmetalfarvestoffer analyseretEn røntgenimpuls sonderer delokaliseringen af jern-3d-elektroner på tilstødende ligander. Kredit:M. Künsting/HZB Overgangsmetalkomplekser i farvestofbaserede solceller er ansvarlige for at omdan -
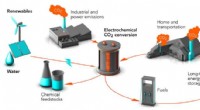 Plast, brændstoffer og kemiske råstoffer fra CO2? De arbejder på detForskere ved Stanford og SLAC arbejder på måder at omdanne kuldioxidaffald (CO2) til kemiske råvarer og brændstoffer, gør en potent drivhusgas til værdifulde produkter. Processen kaldes elektrokemisk
Plast, brændstoffer og kemiske råstoffer fra CO2? De arbejder på detForskere ved Stanford og SLAC arbejder på måder at omdanne kuldioxidaffald (CO2) til kemiske råvarer og brændstoffer, gør en potent drivhusgas til værdifulde produkter. Processen kaldes elektrokemisk -
 Hvordan forskere bekæmper infektionsfremkaldende biofilmEn kunstnerisk skildring af en biofilm med antibiotikaresistente stavformede og sfæriske bakterier. Kredit:Kateryna Kon/Shutterstock.com De overflader, mennesker interagerer med hver dag, kan virk
Hvordan forskere bekæmper infektionsfremkaldende biofilmEn kunstnerisk skildring af en biofilm med antibiotikaresistente stavformede og sfæriske bakterier. Kredit:Kateryna Kon/Shutterstock.com De overflader, mennesker interagerer med hver dag, kan virk -
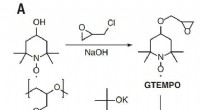 Forskere viser den højeste rapporterede ledningsevne for organisk radikal polymerDen monomersyntese og ringåbningspolymerisationsbaserede syntetiske skema, der bruges til at generere PTEO-radikalpolymeren. Kredit: Videnskab (2018). DOI:10.1126/science.aao7287 Et team af forsk
Forskere viser den højeste rapporterede ledningsevne for organisk radikal polymerDen monomersyntese og ringåbningspolymerisationsbaserede syntetiske skema, der bruges til at generere PTEO-radikalpolymeren. Kredit: Videnskab (2018). DOI:10.1126/science.aao7287 Et team af forsk
- Vurder hvorfor fossiler kan være mere nyttige end stentyper i sammenhængende lag på to forskellig…
- Et bærbart system til overvågning af mavernes aktivitet hele dagen
- Hubble ser hvirvler af danne stjerner
- Forskere udvikler ny test til at opdage sygdom og infektion
- Langt fra pladegrænser kan en vulkan dannes over hot spot?
- Undersøgelsen opfordrer til en genanvendelse af inputsubsidier for at fremme bæredygtig IPM-praksi…


