Ionbinding:Hvilket element danner en ionisk binding med klor (Cl)?
* Ionisk binding: Ionbindinger opstår mellem metaller og ikke-metaller. Metaller har en tendens til at miste elektroner og blive positivt ladede kationer, mens ikke-metaller har tendens til at få elektroner og blive negativt ladede anioner.
* Elektronegativitet: Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner. En stor forskel i elektronegativitet mellem to atomer indikerer en højere sandsynlighed for ionbinding.
Lad os analysere mulighederne:
* Ni (Nikkel): Nikkel er et overgangsmetal, og selvom det kan danne ionbindinger, er det mere sandsynligt, at det danner kovalente bindinger.
* Cu (kobber): Kobber er også et overgangsmetal, og i lighed med nikkel har det en tendens til at danne kovalente bindinger.
* Ga (Gallium): Gallium er et metalloid, hvilket betyder, at det har egenskaber af både metaller og ikke-metaller. Det er mere sandsynligt at danne kovalente bindinger.
* Rb (Rubidium): Rubidium er et alkalimetal. Alkalimetaller er meget reaktive og mister let en elektron for at danne en +1 kation. Klor er et halogen og får let en elektron til at danne en -1 anion. Denne store elektronegativitetsforskel fører til en stærk ionbinding.
Derfor vil chlor bindes ionisk til rubidium for at danne RbCl (Rubidium Chloride).
Sidste artikelFortynde vs. koncentrerede opløsninger:Forstå forskellen
Næste artikelElementer i samme periode som klor:en guide
 Varme artikler
Varme artikler
-
 Forskere opdager en effektiv og bæredygtig måde at filtrere salt- og metalioner fra vand påKredit:CC0 Public Domain Med to milliarder mennesker verden over mangler adgang til rent og sikkert drikkevand, fælles forskning fra Monash University, CSIRO og University of Texas i Austin offent
Forskere opdager en effektiv og bæredygtig måde at filtrere salt- og metalioner fra vand påKredit:CC0 Public Domain Med to milliarder mennesker verden over mangler adgang til rent og sikkert drikkevand, fælles forskning fra Monash University, CSIRO og University of Texas i Austin offent -
 Forskere henter bagergær i jagten på ny medicinGærceller mærket med farverige fluorescerende markører er vist. Kredit:Wikimedia Commons (Public Domain) En af de sværeste dele af opdagelse af lægemidler er at fastlægge, hvordan en medicin fakti
Forskere henter bagergær i jagten på ny medicinGærceller mærket med farverige fluorescerende markører er vist. Kredit:Wikimedia Commons (Public Domain) En af de sværeste dele af opdagelse af lægemidler er at fastlægge, hvordan en medicin fakti -
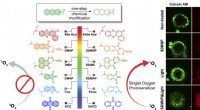 Lab forvandler fluorescerende mærker til kræftdrabereDesignet af thio-baserede fotosensibilisatorer, til venstre, af Rice University viser kemikere løfte om fotodynamisk kræftbehandling, blandt andre applikationer. En thiocarbonylsubstitution - handel m
Lab forvandler fluorescerende mærker til kræftdrabereDesignet af thio-baserede fotosensibilisatorer, til venstre, af Rice University viser kemikere løfte om fotodynamisk kræftbehandling, blandt andre applikationer. En thiocarbonylsubstitution - handel m -
 Ny effektiv katalysator til nøgletrin i kunstig fotosynteseForskningsteamets leder Javier Concepcion (stående, venstre) med Yan Xie, David Shaffer, og David Szalda. Kredit:Brookhaven National Laboratory Kemikere ved det amerikanske energiministeriums Broo
Ny effektiv katalysator til nøgletrin i kunstig fotosynteseForskningsteamets leder Javier Concepcion (stående, venstre) med Yan Xie, David Shaffer, og David Szalda. Kredit:Brookhaven National Laboratory Kemikere ved det amerikanske energiministeriums Broo
- Hvilket udtryk defineres som den proces, hvormed et stof skifter tilstand fra fast stof til væske-?…
- Hvor meget varme genereres af 1700 Joules of Work?
- Lavestfrekvente accreterende millisekund røntgenpulsar fundet
- Hvordan malaria narrer immunsystemet
- Hvad er forholdet mellem ubalancerede styrker og anden bevægelseslov?
- På trods af offentlig forargelse, webadgang for fanger er ikke en luksusartikel - her er hvorfor


